微生物底层能量运行:酶和代谢调控的机制介绍
来源:武汉市灰藻生物科技有限公司 浏览量:115 发布时间:2026-04-29 13:18:41
代谢调控的本质与意义
微生物必须调控代谢,以节约原料和能量,并维持细胞各组分的平衡。
微生物生活的环境中营养、能源和物理条件经常快速变化,需要持续监测内外条件,根据情况激活或关闭代谢途径。
例如,如果某种能源物质不可用,那么利用它的酶就不需要,继续合成这些酶会浪费碳、氮和能量。同样,如果某种终产物已经足够多,微生物还合成制造该产物的酶,那也是极其浪费的。
像大肠杆菌这样的细菌,其调控响应体现了维持平衡、节约能量和物质的驱动力。如果大肠杆菌生长在只含葡萄糖作为碳源和能源的简单培养基中,它会平衡地合成所需的所有细胞组分。
但是,如果在培养基中加入色氨酸,合成色氨酸的途径会立即被抑制,该途径酶的合成也会减慢或停止。同样,如果大肠杆菌转移到只含乳糖的培养基中,它会合成分解乳糖所需的酶。
相反,当大肠杆菌在同时含有葡萄糖和乳糖的培养基中生长时,它会先分解葡萄糖(支持最快生长的糖)。
只有葡萄糖耗尽后,培养物才会利用乳糖。
代谢途径可以,通过三种主要方式进行调控:
1. 代谢分室化:将代谢物和酶定位到细胞不同区域,来影响途径活性。
2. 调控特定酶的合成量:即调控转录和翻译。这两个过程负责合成酶。这种调控相对较慢,但能为细胞节省大量能量和原料。
3. 直接刺激或抑制关键酶活性:这种调控能快速改变途径活性。常被称为翻译后调控,因为它发生在酶合成之后。
本章介绍代谢分室化和酶活性的直接控制。
关于酶合成调控的讨论,放在描述DNA、RNA和蛋白质合成之后,见第12章。
代谢分室化
最常见的代谢分室化机制之一是区室化,即酶和代谢物在不同细胞结构或细胞器中的差异性分布。区室化在真核微生物中尤其重要,因为它们有许多膜结合的细胞器。
例如,脂肪酸分解位于线粒体内,而脂肪酸合成发生在细胞质基质中。原核生物的周质空间也可视为区室化的一个例子。
区室化使得相似途径,可以同时但分开地运行和调控。
此外,通过调控代谢物和辅酶在细胞各区室间的运输,可以协调途径的活性。
假设两个位于不同细胞区室的途径都需要NAD才能活跃。
那么NAD在两个区室间的分布将决定这两个竞争途径的相对活性,获得NAD更多的途径会占优势。
细菌细胞壁(第3.6节);古菌细胞壁(第3.7节)
在细胞质基质等区室内部也存在分室化。
基质是一种结构致密的物质,有许多亚区室。
在真核生物中,它还被内质网和细胞骨架细分。
在这种环境中,代谢物和辅酶扩散不快,因此在局部酶或酶系统附近会形成代谢物梯度。
这是因为特定位置的酶将底物转化为产物,导致某些代谢物浓度降低,另一些升高。
例如,产物浓度在酶附近较高,离酶越远浓度越低。
细胞质基质、微丝、中间丝和微管(第4.3节)
分室化可引起代谢物浓度的显著变化,从而直接影响酶活性。
底物浓度通常在10^{-3}摩尔/升到10^{-6}摩尔/升甚至更低。
因此它们可能与酶浓度处于同一范围,并且等于或小于许多酶的米氏常数(K_m)。
在这些条件下,底物浓度可能控制酶活性,因为底物浓度处于双曲线底物饱和曲线的上升段。
底物水平升高,转化为产物的速度加快;底物浓度下降,酶活性自动降低。
如果不同途径中的两个酶使用同一种代谢物,它们可能直接竞争该代谢物。
赢得竞争的途径——即对该代谢物具有最低K_m值的酶——将更接近满负荷运行。
因此,细胞区室内的分室化,通过代谢物和辅酶水平的变化,来调控和协调代谢。
酶活性的控制
调控酶和其他蛋白质的活性,可以控制许多代谢途径和细胞过程的功能。
这种调控属于翻译后调控,因为它发生在蛋白质合成之后。
有几种翻译后调控机制。有些是不可逆的——例如,蛋白质的切割,可以激活或抑制其活性。
其他类型的翻译后调控是可逆的。
本节中,我们讨论两种重要的可逆控制措施:别构调节(allosteric regulation)和共价修饰(covalent modification)。
我们将重点关注代谢途径的调控,但请记住,并非所有蛋白质或酶都在代谢途径中起作用。
相反,有些参与细胞行为。
本节最后,我们将考虑其中一种行为,趋化性(chemotaxis)的调控。

图 8.21 底物浓度对酶活性的控制
一个酶-底物饱和曲线,标出了米氏常数(K_m)和相当于最大速度(V_max)一半时的速度。反应初速度(v)对底物浓度[底物]作图。最大速度是在固定酶量和特定条件下能达到的最高速度。
当底物浓度等于或小于K_m时,酶活性几乎随底物浓度线性变化。假设底物浓度从A水平增加到B水平。因为这些浓度处于K_m范围内,酶活性会显著增加。浓度从B降到A会降低产物生成速率。
别构调节
大多数调控酶都是别构酶(allosteric enzymes)。
别构酶的活性会被一种叫做效应物(effector)或调节剂(modulator)的小分子改变。
效应物通过非共价力可逆地结合到调控位点(该位点与催化位点分离),并引起酶形状或构象的变化(图8.22)。
催化位点的活性因此改变。
正效应物(positive effector)提高酶活性,负效应物(negative effector)降低酶活性或抑制酶。
这些活性变化通常源于酶对其底物表观亲和力的改变,但也可能发生最大速度的变化。
别构酶的底物饱和曲线通常是S形,而不是非调控酶的双曲线。
因此,调控酶达到其最大速度一半所需的底物浓度有专门的名称:[S]0.5 或 K0.5。
正效应物和负效应物对别构酶K0.5的影响很容易看到,我们以研究最透彻的别构调控酶之一,大肠杆菌的天冬氨酸氨甲酰转移酶(aspartate carbamoyltransferase, ACTase)为例。
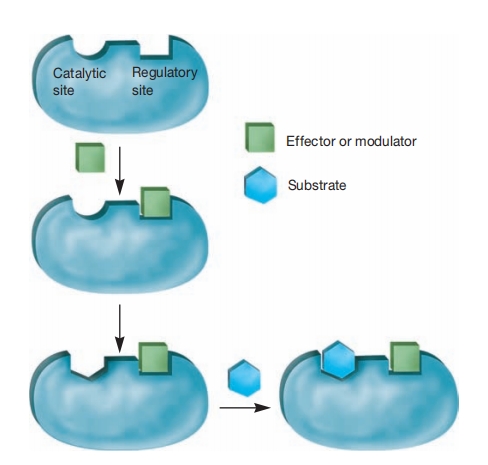
图 8.22 别构调节
别构酶的结构和功能。本例中,效应物或调节剂先结合到单独的调控位点,引起酶构象改变,导致活性位点形状变化。现在活性位点能更有效地结合底物。该效应物是正效应物,因为它刺激底物结合和催化活性。
该酶催化氨甲酰磷酸与天冬氨酸缩合生成氨甲酰天冬氨酸(图8.23)。
这是大肠杆菌嘧啶核苷酸生物合成途径中的限速反应。
当改变任一底物浓度时,底物饱和曲线呈S形(图8.24)。
这是因为该酶有多个活性位点,一个底物分子结合到某个活性位点会增加其他位点对底物的结合。
此外,嘧啶生物合成的终产物三磷酸胞苷(CTP)抑制该酶,而嘌呤ATP激活它。
两种效应物都改变酶的K0.5值,但不改变其最大速度。
CTP通过增加K0.5来抑制(即将底物饱和曲线向右移)。
这导致在特定底物浓度下,有CTP时酶运行更慢。
ATP通过将曲线向左移(向更低底物浓度)来激活酶,使酶在更宽的底物浓度范围内具有最大活性。
因此,当途径过于活跃导致CTP浓度过高时,CTP作为刹车降低ACTase活性。
相反,当嘌呤终产物ATP相对于CTP增加时,它通过对ACTase的作用刺激CTP合成。
嘌呤、嘧啶和核苷酸的合成(第10.6节)

图 8.23 ACTase调控
天冬氨酸氨甲酰转移酶反应及其在嘧啶生物合成调控中的作用。终产物CTP抑制其活性(—),而ATP激活该酶(+)。氨甲酰磷酸合成酶也被途径终产物如UMP抑制。
大肠杆菌天冬氨酸氨甲酰转移酶清楚地展示了别构酶中调控位点和催化位点的分离。
该酶是一个大蛋白,由两个催化亚基和三个调控亚基组成(图8.25)。
催化亚基只含催化位点,不受CTP和ATP影响。
调控亚基不催化反应,但拥有结合CTP和ATP的调控位点。
当这些效应物结合到调控亚基时,它们引起调控亚基和催化亚基的构象变化。
该酶可以在较低活性的T态和较高活性的R态之间可逆转换(图8.25b, c)。
因此,调控位点可以影响约6.0 nm之外的催化位点。
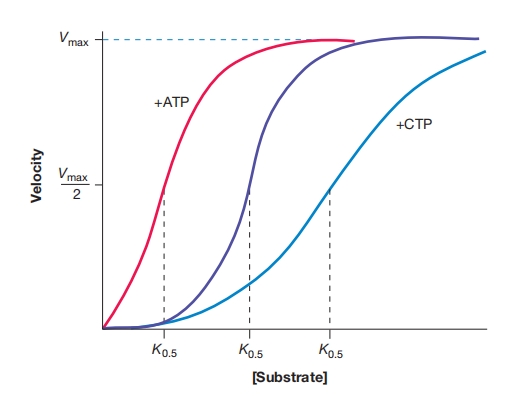
图 8.24 大肠杆菌天冬氨酸氨甲酰转移酶的动力学
负效应物CTP增加K0.5值,正效应物ATP降低K0.5。Vmax保持不变。
酶的共价修饰
调控酶也可以通过可逆的共价修饰(covalent modification)来开启和关闭。
通常通过添加和去除某个特定基团来实现,典型的是磷酸基、甲基或腺苷酰基。
带有附加基团的酶可能被激活或被抑制。
研究最深入的调控酶之一是大肠杆菌的谷氨酰胺合成酶(glutamine synthetase),它参与氮同化。
它是一个由12个亚基组成的大型复合酶,每个亚基都可以被一个腺苷酸残基共价修饰(图8.26)。
当所有12个亚基都连接了腺苷酸残基时,谷氨酰胺合成酶活性不高。
去除AMP基团会产生活性更高的去腺苷酰化谷氨酰胺合成酶,从而生成谷氨酰胺。
氨基酸的合成:氮同化(第10.5节)
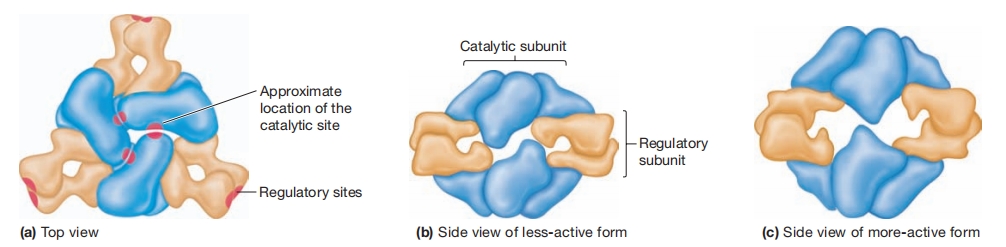
图 8.25 大肠杆菌天冬氨酸氨甲酰转移酶的结构与调控
(a) 酶的结构示意图,显示六个催化链、六个调控链,以及从顶部看的催化位点和调控位点。每个催化亚基包含三个催化链,每个调控亚基有两个链。
(b) ACTase活性较低的T态,侧视图。
(c) ACTase活性较高的R态。调控亚基旋转并推动催化亚基分开。
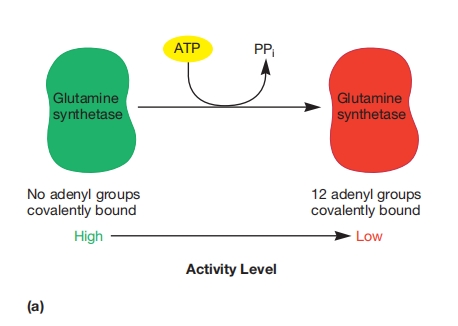
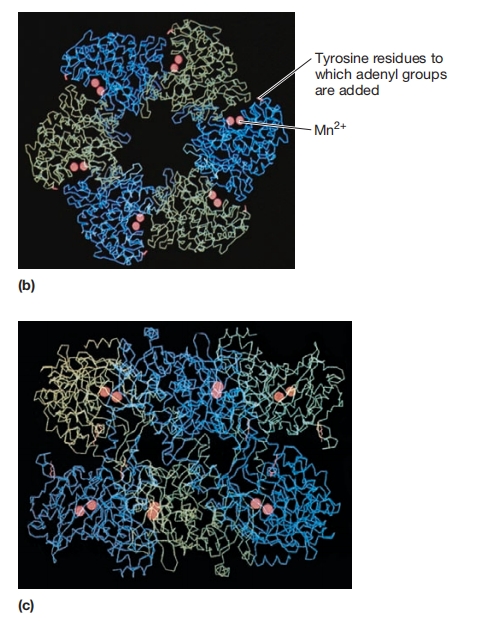
图 8.26 谷氨酰胺合成酶活性的调控
谷氨酰胺合成酶由12个亚基组成,每个亚基可被腺苷酰化。
(a) 随着腺苷酰基数量增加,酶活性降低。
(b) 谷氨酰胺合成酶顶视图,显示12个亚基中的6个。另外6个亚基位于所示6个的正下方。
为清晰起见,亚基交替着色为绿色和蓝色。所示的六个催化位点各有一对Mn2+离子(红圈)。腺苷酰基可连接到每个亚基的特定酪氨酸残基(小红色结构)上。
(c) 侧视图。
使用共价修饰来调控酶活性有一些优点。
这些可相互转换的酶通常也是别构酶。
例如,谷氨酰胺合成酶也受到别构调节。
因为每种形式对别构效应物的反应不同,所以共价修饰酶系统能够以多样而复杂的方式响应更多刺激。
调控也可以作用于催化共价修饰的酶,这给系统增加了第二层调控。
反馈抑制
许多代谢途径的速率是通过控制前述调控酶的活性来调节的。
每条途径至少有一个限速酶(pacemaker enzyme),它催化途径中最慢或限速的反应。
因为其他反应比限速反应进行得更快,所以这个酶活性的变化会直接改变途径的运行速度。
通常途径的第一步是由调控酶催化的限速反应。
途径的终产物常常抑制这个调控酶,这个过程称为反馈抑制(feedback inhibition)或终产物抑制(end product inhibition)。
反馈抑制确保途径终产物的平衡生产。
如果终产物浓度过高,它会抑制调控酶,减慢自身合成。
随着终产物浓度下降,途径活性再次增加,生成更多产物。
这样,反馈抑制自动使终产物供应与需求相匹配。
前面讨论的大肠杆菌天冬氨酸氨甲酰转移酶就是终产物抑制或反馈抑制的一个极好例子。

图 8.27 反馈抑制
具有两个终产物的分支途径中的反馈抑制。分支点酶(催化中间物E转化为F和G的酶)受反馈抑制调节。产物P和Q也抑制途径的初始反应。带有减号末端的彩色线表示终产物P或Q抑制了减号旁边步骤的酶。
通常一条生物合成途径会分支产生多个终产物。
在这种情况下,途径终产物的合成必须精确协调。
不能出现一种终产物过量而另一种缺乏的情况。
分支生物合成途径通常通过使用分支点的调控酶来实现终产物之间的平衡。
如果某种终产物过量,它通常会抑制通向它生成的那个分支上的分支点酶,这样调控自身生成而不影响其他产物的合成。
在图8.27中,注意两个终产物也抑制途径的起始酶。
一种产物过量会减缓碳流入整个途径,同时抑制相应的分支点酶。
因为当一个分支不工作时需要的碳减少,所以对起始限速酶的反馈抑制有助于使供应与分支途径的需求相匹配。
多个分支途径的调控通常因为同工酶(isoenzymes)的存在而更加精细。
同工酶是催化相同反应的不同形式的酶。
起始限速步骤可能由多个同工酶催化,每个同工酶受独立调控。
在这种情况下,单一终产物过量会降低途径活性,但不会完全阻断途径功能,因为有些同工酶仍然活跃。
趋化性
到目前为止,我们讨论酶活性调控时,主要关注通过调节某些途径中调控酶的活性来控制代谢途径。
然而,并非所有酶都在代谢途径中起作用。相反,有些酶参与更复杂的过程。
这些过程包括微生物对环境做出的行为改变。
趋化性(chemotaxis)就是酶在微生物行为中发挥作用的一个例子,以及控制酶活性如何改变该行为。


图 8.28 大肠杆菌趋化反应的蛋白质和信号通路
(a) 甲基接受趋化蛋白(MCPs)形成与CheA和CheW蛋白结合的簇。CheA是一个传感器激酶,被激活后会磷酸化CheB(甲酯酶)或CheY。
磷酸化的CheY与鞭毛马达的FliM蛋白相互作用,导致鞭毛旋转从逆时针(CCW)转为顺时针(CW)。这导致从跑动(CCW旋转)切换到翻滚(CW旋转)。
(b) MCPs、CheW和CheA复合物在细胞两端形成大的受体簇,如这张大肠杆菌电镜照片所示。金标记抗体用于标记受体簇,显示为黑点(圈出)。
(c) 大肠杆菌的趋化信号通路。增加CCW旋转概率的通路以红色显示。CCW旋转是默认旋转。它被引起翻滚的CW旋转周期性打断。
导致CW旋转的通路以绿色显示。灰色分子表示未磷酸化且无活性。注意MCP、CheA和CheZ是同二聚体。CheW、CheB、CheY和CheR是单体。
在第3章中,我们简要介绍了趋化性。
回忆一下,微生物能感知环境中的化学物质,并朝向或远离它们运动,这取决于该化学物质是吸引物(attractant)还是排斥物(repellant)。
为简化讨论,我们只关心朝向吸引物的运动。
研究最透彻的趋化系统是大肠杆菌的。
像许多其他细菌一样,大肠杆菌表现出两种运动模式:向前游动的跑动(run)和翻滚的翻滚(tumble)。
当鞭毛逆时针(CCW)旋转时发生跑动,顺时针(CW)旋转时发生翻滚。
细胞在这两种运动模式间交替,翻滚决定接下来跑动的方向。
当大肠杆菌处于均匀环境中(即所有化学物质浓度在栖息地各处相同),细胞会随机移动,没有明显方向或目的;这称为随机行走(random walk)。
但如果环境中存在化学梯度,只要细胞朝向吸引物移动,翻滚的频率就会降低。
换句话说,朝向吸引物移动的时间增加了,最终细胞更靠近吸引物。
不过这个过程并不完美。因为细菌很小,它们常常被环境中分子的运动撞离路线。
因此它们必须通过翻滚介导的试错过程不断调整方向。
观察细胞行进的路径,它类似于随机行走,但偏向吸引物。
因此细菌朝向吸引物的运动常被称为偏向随机行走(biased random walk)。
三十多年来,科学家一直在剖析这种复杂行为,以理解大肠杆菌如何感知吸引物存在,如何从跑动切换到翻滚再切换回来,以及如何知道它正朝着正确方向前进。
趋化性的许多方面现在已被了解(至少是表面上的),但仍有许多问题未解。
但有一点很清楚:大肠杆菌的趋化反应涉及许多通过共价修饰调控的酶和其他蛋白质。
一个重要组成部分是磷酸转移系统(phosphorelay system)。
磷酸转移系统至少包含两种蛋白质:一个传感器激酶(sensor kinase)和一个反应调节蛋白(response regulator)。
这里描述的磷酸转移系统用于调控酶活性。
其他磷酸转移系统用于调控蛋白质合成,通常只使用这两个组分。这些系统在第12章中介绍。
为了让趋化发生,大肠杆菌必须判断是否有吸引物存在,然后调节决定鞭毛旋转方向(跑动或翻滚)的磷酸转移系统的活性。
大肠杆菌通过化学物质结合到趋化受体来感知环境中的化学物质。
已鉴定出许多趋化受体。我们重点关注一类称为甲基接受趋化蛋白(methyl-accepting chemotaxis proteins, MCPs)的受体。
控制鞭毛旋转方向的磷酸转移系统包括传感器激酶CheA和反应调节蛋白CheY。
当被激活时,CheA利用ATP自身磷酸化。
磷酸基团随后迅速转移到CheY。
磷酸化的CheY通过细胞质扩散到鞭毛马达。
与马达相互作用后,旋转方向从CCW切换为CW,从而发生翻滚。
当CheA无活性时,鞭毛以默认模式(CCW)旋转,细胞向前平滑跑动。
如上所述,MCPs的状态必须传递给CheA/CheY磷酸转移系统。这是如何实现的?
MCPs埋在质膜中,不同部分暴露在膜的两侧。
每个MCP的周质侧有一个或多个吸引物分子的结合位点。
MCP的细胞质侧与两种蛋白CheW和CheA相互作用。
CheW蛋白结合MCP并帮助附着CheA蛋白。
MCP受体与CheW和CheA一起在细胞的一个或两个极形成大的簇。
据认为,MCPs、CheA和CheW的较小聚集体(作为信号团队)是受体簇的构建模块。
信号团队中各分子的数量尚不清楚,但有人提出每个团队包括三个受体(通常不同类型)、两个CheW分子和一个CheA二聚体。
也有人提出信号团队彼此聚集形成“信号联盟”。
最后,信号团队(也许还有信号联盟)通过未知机制相互连接,形成在细胞极可见的受体簇。
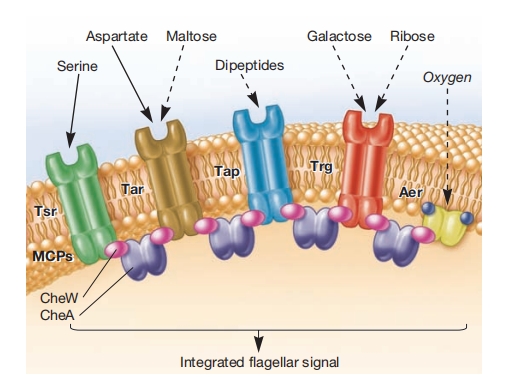
图 8.29 大肠杆菌的甲基接受趋化蛋白
每个甲基接受趋化蛋白(MCP)感知的吸引物如图所示。有些是直接感知的,即吸引物结合MCP(实线)。其他是间接感知的(虚线)。
吸引物麦芽糖、二肽、半乳糖和核糖通过与周质结合蛋白的相互作用被检测到。氧气被Aer趋化受体间接检测,该受体与其他MCP不同,它缺乏周质感知结构域。
相反,其细胞质结构域有一个FAD结合位点。FAD是许多电子传递链中的重要电子载体。MCP结合的FAD分子的氧化还原状态用于监测电子传递系统的功能。这反过来介导对氧气的趋化反应。
无论受体簇的确切化学计量或结构如何,有证据表明每个信号团队中的MCPs协同工作以调节CheA活性。
当信号团队中任何一个MCP结合了吸引物时,CheA自身磷酸化被抑制,鞭毛继续CCW旋转,细胞继续跑动。
由于这种协作,细胞能对极低浓度的吸引物做出反应。
此外,它可以整合团队中所有受体的信号(图8.29)。
另一方面,如果吸引物水平下降,导致信号团队中结合吸引物的MCPs减少,CheA被刺激发生自身磷酸化,磷酸转移级联启动,细胞开始翻滚。
但翻滚不会无限持续。在切换到CW旋转后约10秒,CheZ蛋白从CheY上去除磷酸基团,CCW旋转恢复。
但是,大肠杆菌如何测量环境中吸引物的浓度?它如何知道正在朝向吸引物移动?
大肠杆菌每隔几秒测量一次吸引物浓度,并判断浓度是随时间增加还是减少。
只要浓度增加,细胞就继续跑动。如果浓度减少,就会触发翻滚。
为了比较不同时间的吸引物浓度,大肠杆菌必须有记住先前浓度的机制。
大肠杆菌通过比较MCPs(细胞质侧)的整体甲基化水平与结合吸引物(周质面)的整体数量来实现这一点。
每个MCP的细胞质部分有4到6个可被甲基化的谷氨酸残基。
甲基基团的添加和去除由两种不同的酶催化。
甲基化由MCP特异性甲基转移酶(methyltransferase)CheR催化。
去甲基化由MCP特异性甲酯酶(methylesterase)CheB催化。
无论吸引物水平如何,甲基化都以相当稳定的速率发生。
但是,MCP-吸引物复合物是CheR更好的底物,比未结合吸引物的MCP更优。
因此当吸引物结合时,MCP的甲基化更有利。
CheB的甲酯酶活性也受CheA蛋白的修饰。
只要吸引物浓度持续增加,结合吸引物的MCPs数量保持高位,MCP甲基化水平也保持高位。
然而,如果吸引物浓度下降,甲基化水平将超过结合吸引物的MCPs水平。
这种甲基化水平与MCP结合吸引物之间的差异会刺激CheA自身磷酸化。
结果,启动CW鞭毛旋转的磷酸转移信号产生,细胞翻滚,试图在梯度中重新定向,使其朝向吸引物(上梯度)而非远离吸引物(下梯度)移动。
同时,CheA上的一些磷酸基团转移到CheB。这激活了CheB,它从MCPs上去除甲基。
这降低了甲基化水平,使其与结合吸引物的MCPs数量相称。
几秒钟后,结合吸引物的MCPs数量将与这个新的甲基化水平进行比较。
基于两者的对应关系,细胞将判断是否再次朝向上梯度移动。
如果是,翻滚将被抑制(甲酯酶活性也被抑制),跑动继续。
参考文献
https://www.mun.ca/biology/scarr/Principle_of_RT-PCR.html
http://www.primerdesign.co.uk/assets/files/beginners_guide_to_real_time_pcr.pdf
相关产品
HZB325136:新型隐球酵母ATCC 32045(血清型:D) | Cryptococcus neoformans (Serotype:D)
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-04-20
编制人:小藻
审稿人:小藻
