微生物底层能量运行:酶和代谢调控的本质
来源:武汉市灰藻生物科技有限公司 浏览量:86 发布时间:2026-03-29 17:28:05
“酶”的重要性
回顾一下,放能反应是ΔG°′为负、平衡常数大于1的反应。 放能反应会按反应式方向(即方程右侧)进行完全。
然而,人们通常将放能反应的反应物混合后,却观察不到明显的结果。
例如,多糖水解为单糖是放能的,且会自发进行。 但有机化学家需要在6 M盐酸和100℃条件下进行数小时,该反应才能进行完全。
而细胞可以在中性pH、更低的温度下,仅在几分之一秒内完成相同的反应。 细胞是如何做到的?
它们能这样做,是因为它们制造了称为“酶”的蛋白质,这些蛋白质能加速化学反应。
酶对细胞至关重要,因为没有它们,大多数生物反应进行得非常缓慢。 事实上,酶使生命成为可能。
酶的结构与分类
酶可以定义为,蛋白质催化剂,对所催化的反应和作用的分子,具有高度的特异性。 催化剂是能提高化学反应速率,而自身不被永久改变的物质。
因此,酶能加速细胞反应。 发生反应的分子称为底物,形成的物质称为产物。
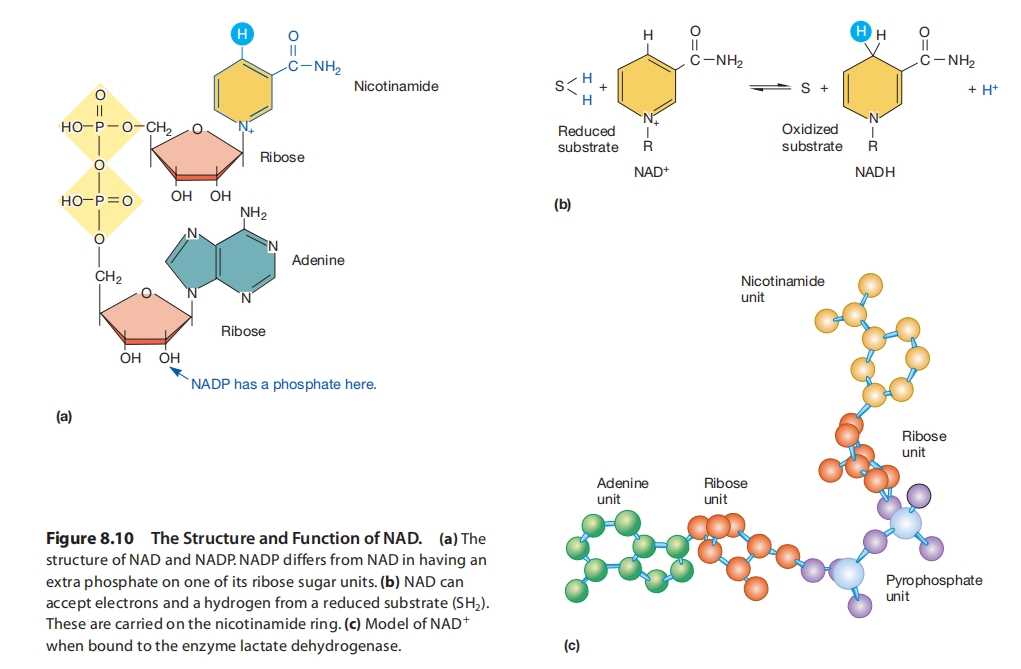
NAD的结构与功能:
(a)NAD和NADP的结构。NADP与NAD的区别在于其一个核糖单位上多了一个磷酸基团。
(b)NAD可以从还原性底物(SH₂)接受电子和一个氢。这些基团由烟酰胺环携带。
(c)NAD⁺结合于乳酸脱氢酶时的模型。
许多酶仅由蛋白质组成。 然而,有些酶由蛋白质部分(脱辅基酶蛋白)和催化活性所需的非蛋白质组分(辅因子)共同组成。
由脱辅基酶蛋白及其辅因子组成的完整酶称为全酶。 如果辅因子与脱辅基酶蛋白牢固结合,则称为辅基。
如果辅因子与脱辅基酶蛋白松散结合,并在产物形成后可从蛋白质上解离,则称为辅酶。 许多辅酶可以将某一种产物携带至另一种酶。
尽管细胞中的酶数量庞大、种类繁多,但它们可以分为六大类。 酶通常根据其作用的底物和催化的反应类型来命名。 例如,乳酸脱氢酶(LDH)从乳酸中移除氢。
乳酸 + NAD⁺ ⇌ 丙酮酸 + NADH + H⁺
乳酸脱氢酶也可以给出更完整、详细的名称:L-乳酸:NAD⁺ 氧化还原酶。 该名称更精确地描述了底物和反应类型。
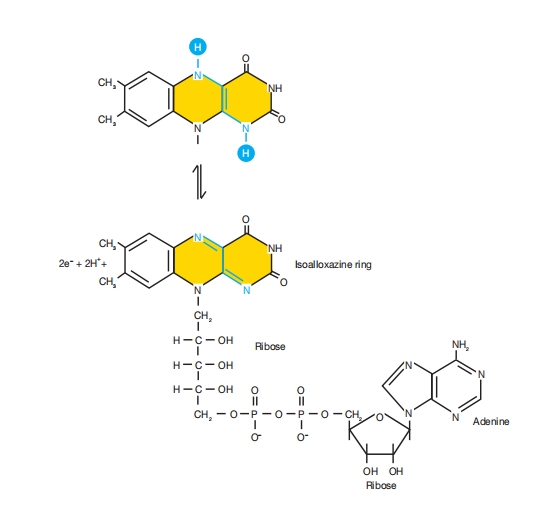
FAD的结构与功能: 维生素核黄素由异咯嗪环及其连接的核糖组成。FMN是核黄素磷酸。环中直接参与氧化还原反应的部分以彩色显示。
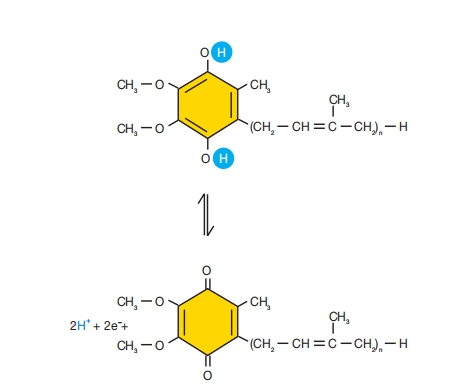
辅酶Q(泛醌)的结构与功能:侧链长度因生物而异,n = 6 至 n = 10。
酶的分类
| 酶的类型 | 催化的反应 | 反应示例 |
|---|---|---|
| 氧化还原酶 | 氧化还原反应 | 乳酸脱氢酶:丙酮酸 + NADH + H⁺ ⇌ 乳酸 + NAD⁺ |
| 转移酶 | 分子间基团转移反应 | 天冬氨酸氨甲酰转移酶:天冬氨酸 + 氨甲酰磷酸 → 氨甲酰天冬氨酸 + 磷酸 |
| 水解酶 | 分子水解反应 | 葡萄糖-6-磷酸酶:葡萄糖-6-磷酸 + H₂O → 葡萄糖 + Pi |
| 裂合酶 | 移除基团形成双键或向双键添加基团 | 延胡索酸水合酶:L-苹果酸 ⇌ 延胡索酸 + H₂O |
| 异构酶 | 异构化反应 | 丙氨酸消旋酶:L-丙氨酸 ⇌ D-丙氨酸 |
| 连接酶 | 利用ATP能量连接两个分子 | 谷氨酰胺合成酶:谷氨酸 + NH₃ + ATP → 谷氨酰胺 + ADP + Pi |
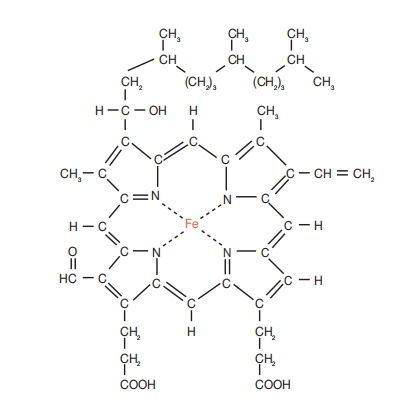
血红素的结构: 血红素由卟啉环和一个连接的铁原子组成。它是许多细胞色素的非蛋白质成分。铁原子交替接受和释放一个电子。
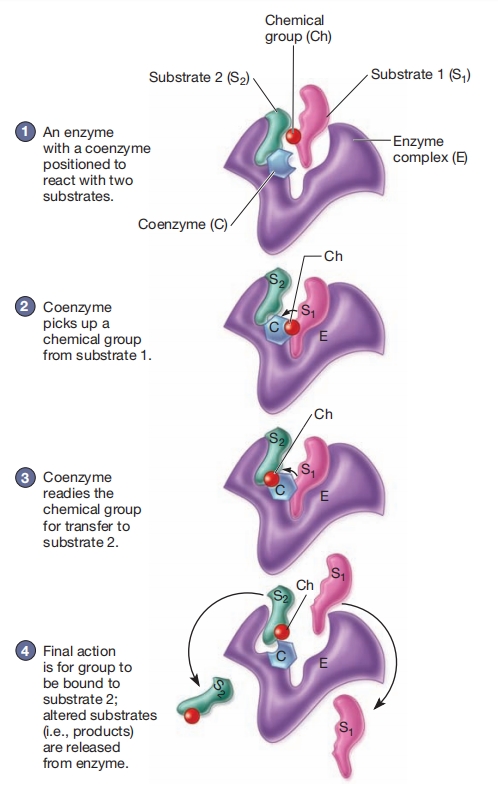
作为载体的辅酶: 一种带有辅酶的酶,准备与两种底物反应。
酶的作用机制
需要记住,酶能提高反应速率,但不改变反应的平衡限制。 如果反应是吸能的,酶的存在不会改变其平衡以生成更多产物。 酶只是加快了反应向其最终平衡状态前进的速度。
酶是如何催化反应的? 尽管完整答案复杂冗长,但通过考察一个简单的放能化学反应过程,可以理解部分机制。
A + B → C + D
当分子A和B相互接近准备反应时,它们会形成一个过渡态复合物,该复合物兼具底物和产物的特征。 需要活化能将反应分子以正确方式聚集在一起以到达过渡态。
过渡态复合物随后可以解离生成产物C和D。 反应物与产物之间的自由能差即为ΔG°′。 因此,在我们的例子中,由于ΔG°′为负(即产物能量水平低于底物),平衡将倾向于产物。
如图8.15所示,如果不为A和B提供相当于活化能的能量,它们将不会转化为C和D。 酶通过降低活化能来加速反应;
因此,更多的底物分子将有足够的能量聚集在一起形成产物。 尽管平衡常数(或ΔG°′)不变,但由于活化能降低,在酶存在时,平衡能更快达到。
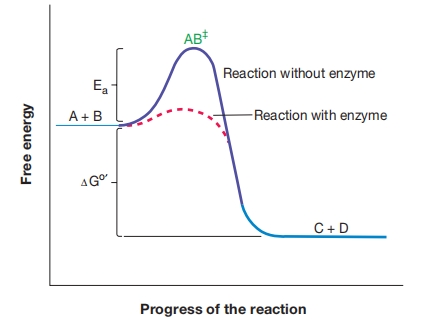
活化能与酶功能。 活化能是反应物达到过渡态所需的能量。由于ΔG°′为负,平衡偏向产物。酶通过降低活化能来加速反应。
研究人员一直致力于揭示酶如何降低反应的活化能,这一过程正变得越来越清晰。 酶在其表面称为活性位点或催化位点的特定位置将底物聚集在一起,形成酶-底物复合物。
酶与底物相互作用的方式主要有两种。 酶可能是刚性的,形状与底物精确匹配,以便正确的底物特异性结合并正确定位以进行反应。
这种机制称为“锁钥”模型。 酶也可能在与底物结合时改变形状,使活性位点包围并精确匹配底物。 这被称为“诱导契合”模型,已糖激酶和许多其他酶都采用这种机制。
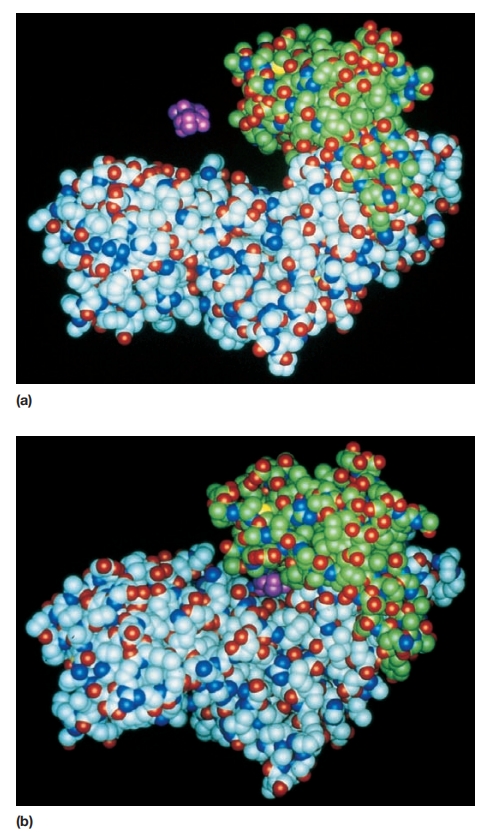
酶功能的诱导契合模型。
(a)酵母己糖激酶(绿色和蓝色小叶)及其底物葡萄糖(紫色)的空间填充模型。活性位点位于酶的小叶和大叶形成的裂缝中。
(b)当葡萄糖结合形成酶-底物复合物时,己糖激酶改变形状并包围底物。
酶-底物复合物的形成可以通过多种方式降低活化能。 例如,通过在活性位点将底物聚集在一起,酶实际上浓缩了底物,从而加快了反应速度。
然而,酶不仅仅浓缩其底物。 它还能结合底物,使它们彼此之间正确定向,以形成过渡态复合物。 这种定向降低了底物达到过渡态所需的能量。
这些以及其他催化位点活动能将反应速率加快数十万倍。
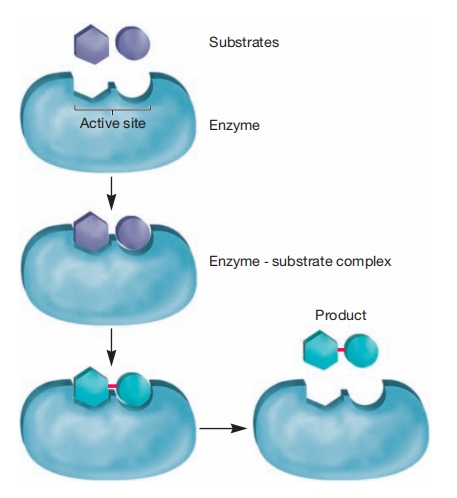
酶功能的锁钥模型。 在此模型中,活性位点是一个相对刚性的结构,仅容纳具有正确对应形状的分子。图中显示了酶-底物复合物的形成及其向产物的转化。
环境对酶活性的影响
酶活性随环境因素的变化而有很大差异,最重要的因素之一是底物浓度。 正如后续将强调的,细胞内的底物浓度通常很低。
在底物浓度非常低时,酶生成产物的速度很慢,因为它很少能接触到底物分子。
如果存在更多底物分子,酶与底物结合的机会增加,反应速度(通常以产物形成速率表示)会比在较低底物浓度时更高。
因此,酶促反应速率随底物浓度增加而增加。 最终,进一步提高底物浓度并不会导致更大的反应速度,因为现有的酶分子已尽可能快地结合底物并将其转化为产物。
也就是说,酶被底物饱和,并以最大速度运行。 由此产生的底物浓度曲线是双曲线。 了解酶正常运作所需的底物浓度是有用的。
通常,使用米氏常数(Km,即酶达到最大速度一半时所需的底物浓度)来衡量酶对其底物的表观亲和力。
Km值越低,酶催化其反应所需的底物浓度就越低。
Km值低的酶被称为对其底物具有高亲和力。
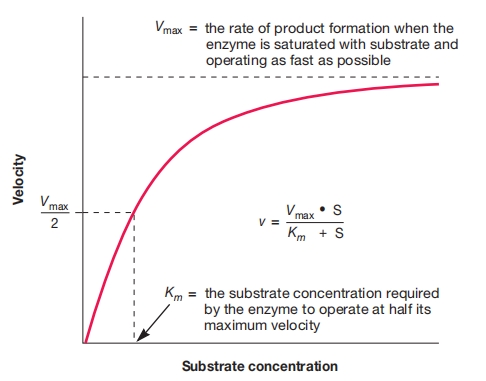
米氏动力学。 酶活性对底物浓度的依赖性。该底物曲线符合图中给出的米氏方程,该方程使用最大速度和米氏常数(Km)将反应速度与底物浓度相关联。
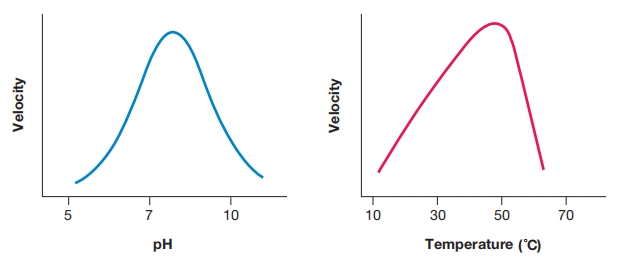
pH、温度与酶活性。 酶活性随pH和温度的变化。pH和温度的范围仅为示意。不同酶的最适点位置以及pH和温度曲线的形状各不相同。
酶的活性也随pH和温度的变化而改变。 每种酶在特定的最适pH下运行最快。 当pH偏离酶的最适值太远时,活性减慢,酶可能受损。 酶同样具有最适温度以达到最大活性。 如果温度上升到超过最适值太多,酶的结构会被破坏,其活性丧失。 这种称为变性的现象可能由极端的pH和温度或其他因素引起。 微生物酶的最适pH和最适温度通常反映了其生境的pH和温度。 毫不奇怪,在高温下生长最佳的细菌通常具有高最适温度和高度热稳定性的酶。
酶的抑制
微生物可被多种化学物质毒害,许多最有效的毒物都是酶的抑制剂。
竞争性抑制剂在酶的催化位点直接与底物竞争,阻止酶形成产物。 竞争性抑制剂通常与正常底物相似,但不能被转化为产物。
竞争性抑制剂在治疗许多微生物疾病中很重要。 磺胺类药物如磺胺类似于对氨基苯甲酸(PABA),这是一种用于合成辅酶叶酸的分子。
这些药物与对氨基苯甲酸竞争参与叶酸合成的酶的催化位点。 这阻断了叶酸的生成,从而抑制细菌生长。 人类不受伤害,因为人类不合成叶酸,而是从饮食中获取。
非竞争性抑制剂也能通过与活性位点以外的位置结合来影响酶活性。 这会改变酶的形状,使其失活或活性降低。
这些抑制剂被称为非竞争性,因为它们不直接与底物竞争。 重金属毒物如汞通常是酶的非竞争性抑制剂。
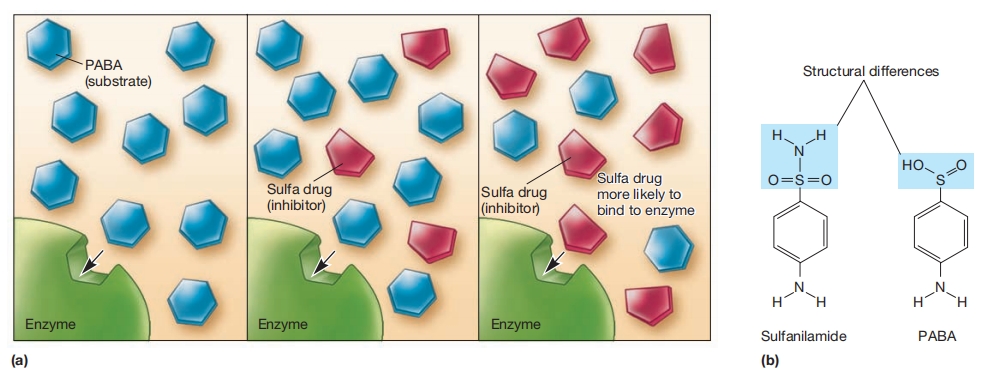
酶活性的竞争性抑制
(a)竞争性抑制剂通常在形状上与正常底物相似,因此能与酶的活性位点结合。这阻止了底物结合,反应被阻断。
(b)磺胺的结构,PABA的结构类似物。PABA是参与叶酸生物合成的一种酶的底物。当磺胺与该酶结合时,酶活性被抑制,叶酸合成停止。
代谢调节的本质与意义
微生物必须调节其代谢,以节约原料和能量,并在各种细胞组分之间维持平衡。
由于它们生活的环境中营养物质、能源和物理条件常常迅速变化,因此必须持续监测内部和外部条件并做出相应反应。 这涉及根据需要激活或失活代谢途径。
例如,如果某种特定能源不可用,则利用该能源所需的酶就不再需要,进一步合成它们是对碳、氮和能量的浪费。
如果某种最终产物已经足够,微生物还去合成制造该产物所需的酶,将是极其浪费的。
维持平衡、节约能量和物质的驱动力在大肠杆菌等细菌的调节反应中显而易见。
如果该细菌在仅含葡萄糖作为碳源和能源的极简单培养基中生长,它会以平衡的量合成所有必需的细胞组分。
然而,如果向培养基中添加氨基酸色氨酸,合成色氨酸的途径将立即受到抑制,该途径酶的合成也会减慢或停止。
如果将大肠杆菌转移到仅含乳糖的培养基中,它会合成分解代谢这种营养物质所需的酶。
相比之下,当大肠杆菌在同时含有葡萄糖和乳糖的培养基中生长时,它会先分解代谢葡萄糖(支持最快生长的糖),只有在葡萄糖耗尽后才会利用乳糖。
代谢途径可以通过三种主要方式进行调节:
- 代谢分室化——通过将代谢物和酶定位到细胞的不同部分来影响途径活性。
- 调节特定酶的合成量——换言之,可以调控转录和翻译。这两个过程负责合成酶。这种水平的调节相对较慢,但能为细胞节省大量能量和原料。
- 直接刺激或抑制关键酶的活性——这种调节方式能快速改变途径活性。它通常称为翻译后调节,因为它发生在酶合成之后。
参考文献
《Microbiology (Seventh Edition)》 | 微生物学(第七版),第8节
相关产品
| 货号 | 名称 | 价格 | 规格 |
|---|---|---|---|
| HZB875586 | 碎肉碳水化合物肉汤培养基 | 350 | 250g/瓶 |
| HZB875648 | 庖肉牛肉粒 | 230 | 100g/瓶 |
| HZB875647 | 氯化血红素 | 60 | 5ml/支(0.1mg/ml)、5支/盒 |
| HZB875646 | 维生素K1 | 50 | 5ml/支(1mg/ml)、5支/盒 |
| HZB875650 | L-半胱氨酸盐酸溶液 | 60 | 1ml/支(0.05g/ml),5支/盒 |
敬请关注灰藻生物,共筑健康未来!— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-03-31
编制人:小藻
审稿人:小藻
