分子实验笔记09:聚合酶链式反应(Polymerase Chain Reaction, PCR)和测序验证
来源:武汉市灰藻生物科技有限公司 浏览量:176 发布时间:2026-03-10 21:03:05
引言(Introduction)
标准PCR(Polymerase Chain Reaction)是一种体外(in vitro)扩增技术,可利用Taq DNA聚合酶(Taq Polymerase)对DNA分子中某一特定短片段(例如单个基因)进行指数级复制。
仅需一份DNA模板(template),研究者即可通过一套简单的试剂和反复的加热-冷却循环(即变性与退火),获得数千份完全相同的拷贝。
该技术的自动化得益于从嗜热菌Thermus aquaticus中分离出的耐热DNA聚合酶——Taq酶。Taq酶能耐受多次高温变性循环,而其他来源的DNA聚合酶在此条件下会失活。
除模板DNA和Taq聚合酶外,PCR反应还需以下组分:
- 脱氧核苷三磷酸(dNTPs):包括腺嘌呤(A)、胞嘧啶(C)、鸟嘌呤(G)和胸腺嘧啶(T),以等摩尔比例提供DNA合成原料;
- 两条特异性单链DNA引物(oligonucleotide primers):分别与目标片段上游(5′端)和下游(3′端)互补结合。
当上述组分在合适缓冲液中混合后,通过一系列变性(denaturation)步骤,Taq聚合酶即可在引物之间合成新的DNA链。
经过多轮循环,仅需几纳克(ng)模板DNA,即可产出数微克(μg)的目标DNA产物。
PCR完成后,可通过琼脂糖凝胶电泳(agarose gel electrophoresis)根据片段大小验证扩增结果。
基础PCR程序(Basic PCR Program)
- 初始变性(Initial Denaturation):94°C,2分钟
使双链DNA模板充分解链,破坏碱基对间的氢键。此步通常在94–98°C进行。 - 变性(Denature):94°C,30秒
持续维持双链DNA解离状态。 - 退火(Anneal primers):55°C,30秒
正向与反向引物在此温度下稳定结合至单链DNA模板两端;同时,Taq聚合酶亦可稳定结合至引物-DNA复合物。 - 延伸(Extend DNA):72°C,1分钟
Taq聚合酶的最适活性温度为70–75°C,此步骤使其高效、准确地合成新链。 - 重复步骤2–4共25–30个循环。
- 最终延伸(Final Extension):72°C,5分钟
补平新合成DNA链的突出末端,确保产物完整性。
材料清单(Materials List)
每50 μL PCR反应所需试剂:
- 薄壁PCR管(Thin-walled PCR tube)
- 冰盒(Ice Bucket)
- 模板DNA(Template DNA):2 μL(10–500 ng)
- 10× Taq缓冲液(含MgCl₂):5 μL
- dNTP混合液(各10 mM):1 μL
- 正向引物(Forward Primer,10 μM母液):2.5 μL
- 反向引物(Reverse Primer,10 μM母液):2.5 μL
- 无菌去离子水(Sterile dH₂O):36.8 μL(可调)
- Taq DNA聚合酶(5 U/μL):0.2 μL
- PCR仪(PCR Machine)
- 琼脂糖凝胶(Agarose Gel)
操作流程(Procedure)
引物设计与PCR(Primer Design and PCR)
- 设计引物。参见我们的引物设计protocol。
注: 是一款优秀的引物设计工具。 - 将薄壁PCR管置于冰上。
- 配制50 μL反应体系(所有试剂保持在冰上):
- 将反应管放入PCR仪。
- 将退火温度设为引物熔解温度(Tm)低5°C。
- 延伸时间按产物长度设定:普通Taq酶为每kb 1–2分钟;若使用具校对功能(proofreading)的高保真酶,请参考厂商说明。
- 运行以下程序:
- 取2 μL PCR产物进行琼脂糖凝胶电泳,验证片段大小与产量。
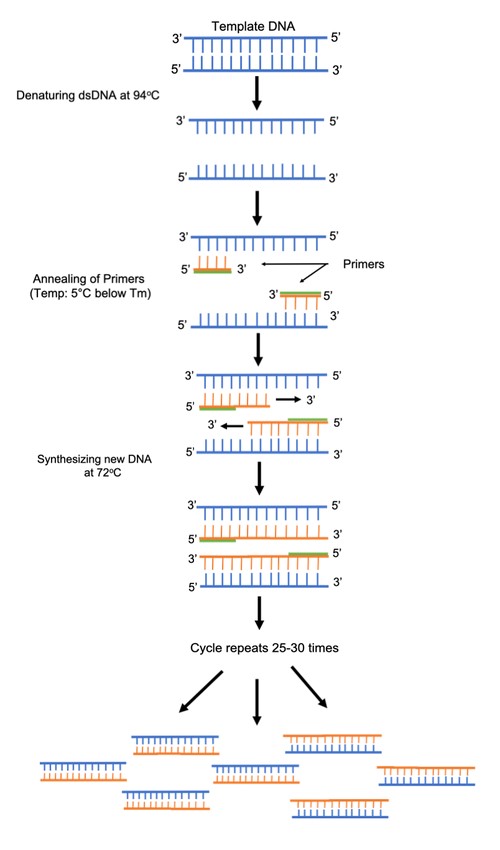
图1:PCR扩增流程示意图
主混合液配制(Master Mix Preparation)
- 将每种试剂体积乘以反应数,并额外增加10%以补偿移液误差。例如:7个不同引物对 → ×7。
- 在1.5 mL离心管中混合以下组分:
- 轻柔吹打混匀,全程保持在冰上。
- 先向各PCR管中分别加入正、反向引物(各2.5 μL)。
技巧:将正向引物加在一侧管壁,反向引物加在另一侧,便于确认已加。 - 向每管加入45 μL主混合液(50 μL总体系 – 2.5 μL正向引物 – 2.5 μL反向引物)。
- 盖紧管盖,轻弹管底使液体汇集,再放入PCR仪。
引物稀释(Diluting Primers)
多数引物由公司合成并以冻干粉形式提供。使用者需用无菌dH₂O重悬。
- 配制100 μM母液:加入的dH₂O体积(μL)= 引物nmol数 × 10。
例:38.5 nmol引物 → 加385 μL水。 - 立即配制10 μM工作液:取100 μL 100 μM母液 + 900 μL dH₂O(1:10稀释)。
技巧与常见问题(Tips and FAQ)
技巧(Tips)
- 若目标序列GC含量高,可适当延长变性时间。
- 正、反向引物的熔解温度(Tm)应尽量接近。退火温度设为Tm – 5°C;若出现非特异性条带,可逐步提高退火温度1–2°C。
- DNA合成速率约为1–2 kb/分钟,延伸时间应根据目标片段长度调整。
如何设计引物?
请参阅我们的引物设计指南。如用于克隆,请参考“基于PCR的质粒克隆”实验流程。
PCR失败怎么办?
尝试在每管中加入: - 1 μL 25 mM MgCl₂(补充缓冲液中可能因冻融损失的Mg²⁺); - 和/或 1 μL DMSO(有助于GC-rich模板变性)。
建议设置三组对照:仅加MgCl₂、仅加DMSO、两者都加。
各组分作用详解:
- 模板DNA(Template DNA):
含有待扩增的目标序列,必须与引物互补才能有效扩增。 - Taq缓冲液(含MgCl₂):
为聚合酶提供最佳化学环境。Mg²⁺等二价阳离子可稳定反应体系;高浓度会提高聚合酶错配率,亦可用于PCR介导的定点突变。 - dNTPs:
DNA合成的基本单元,由聚合酶逐个添加至新生链。 - 正向与反向引物:
分别与模板DNA正义链和反义链3′端互补,作为DNA合成的起始点。 - Taq DNA聚合酶:
耐热型DNA聚合酶,最适温度约70°C,负责催化新链合成。 - 无菌dH₂O:
补足反应体积,提供适宜溶剂环境。
序列验证
序列验证(sequence verification),例如插入基因(gene/insert)、融合蛋白(fusion proteins)、点突变(point mutations)、缺失(deletions)等,需要选择一个或多个特异性寡核苷酸引物(oligonucleotide primers),这些引物应位于待验证区域的两侧(即“侧翼”)。
在选择测序引物时,需考虑以下因素:
- 引物是否唯一?
确保该引物在整个质粒构建体(construct)中仅有一个结合位点(anneals once)。 - 引物与目标区域的距离是否合适?
引物应距离目标区域至少50个核苷酸(nt),最多不超过300个核苷酸。过近或过远都会影响测序质量。 - 是否有商业化通用引物可用?
许多常用引物(如M13F、M13R、T7、SP6等)已整合在常见质粒骨架(plasmid backbone)中。多数测序平台(sequencing core)会提供一份免费通用引物列表,可直接选用而无需额外费用。
一次良好的测序反应通常可获得300–900个碱基对(bp)的高质量可用序列。您将收到一个测序峰图文件(trace file,格式为.ab1),
该文件以彩色峰图形式直观展示序列:每种颜色代表一种核苷酸碱基(A、T、C、G)。
下图展示了一段高质量测序反应的典型峰图示例:
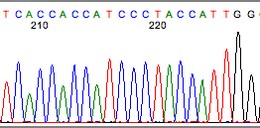
高质量测序反应样本的测序结果文件示例
需要注意的是,测序反应起始和末端区域的序列往往不可靠。尽管测序结果可能给出了具体碱基,但通过查看峰图(trace file)会发现这些碱基判读(base calls)可信度低。
下图展示了一段背景噪音高、信号混乱的测序峰图:
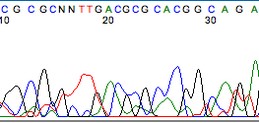
杂峰,信号差
我可以用什么软件查看 .ab1 峰图文件?
有多款免费软件支持打开 .ab1 文件,例如:
- 4Peaks(Mac)
- SnapGene Viewer(Mac/PC)
- FinchTV(Mac/PC)
- Sequence Scanner(PC)
- Chromas(PC)
如何判断某个碱基峰是否被错误判读?
打开 .ab1 峰图文件,使用软件中的搜索功能定位到可疑序列位置,仔细观察该区域的峰形。可靠的碱基应表现为单一、清晰、高度适中且无重叠的峰。
例如,在下方峰图中,70号碱基之后出现了同一位置的多重峰(multiple peaks),表明此处可能存在杂合、插入或测序错误。仅看碱基序列文本容易误判,而峰图能提供更真实的信息。
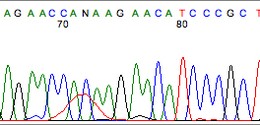
重叠峰
我的序列中出现了“N”,这是什么意思?
“N”是IUPAC标准中表示任意碱基(any of the four bases: A/T/C/G)的符号,通常意味着测序软件无法确定该位置的确切碱基。此时应:
- 打开 .ab1 峰图文件,手动检查该位置的信号;
- 若峰形单一清晰,可自行判读正确碱基;
- 若峰形模糊或重叠,“N”可能是由测序反应中的错误插入、模板不纯或信号衰减导致。
参考文献
https://www.addgene.org/
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-02-09
编制人:磊子
审稿人:小藻
