利用金属-酚网络保护厌氧微生物免受加工影响
来源:武汉市灰藻生物科技有限公司 浏览量:23 发布时间:2026-04-30 13:27:13
摘要
肠道微生物组对维持健康和预防疾病至关重要。微生物生物治疗药物,对于解决这些问题很重要,但它们在给药时必须保持活性才有效。
许多有潜在治疗价值的物种是厌氧菌,受限于保护方法效果,它们难以生产。
我们开发了一种细胞涂层,用于提高下一代生物治疗药物 Bacteroides thetaiotaomicron 的活性和稳定性。
该涂层能保护微生物免受苛刻加工条件和氧气暴露的影响,即使在缺乏典型冷冻保护剂的情况下也是如此。这一进展将扩大,可稳定生产的微生物范围,促进新兴菌株的开发。
引言
肠道微生物负责多种过程,包括合成必需维生素、分解纤维素,以及防止病原体入侵。当这个群落失衡时,可能导致从过敏到癌症等问题,如胃肠道感染,每年造成600万人死亡。
鉴于微生物在人类健康中的关键作用,迫切需要将其开发为生物治疗药物,以维持肠道稳态、治疗疾病并保持或恢复屏障功能。
微生物治疗药物生产中,关键是在给药时必须保持活性。目前,大多数益生菌是,基于易于生产的原则,从少数几个物种中生产出来的。
但是,随着对微生物组认识的深入,需要新的微生物补充剂来维持健康,或作为生物治疗药物。
然而,关键的菌株是厌氧菌,由于现有保护策略存在局限,用现有技术几乎无法生产它们。厌氧菌的制造尤其困难,原因是氧气毒性和生产过程中的损伤。
虽然干燥储存通常是给药所必需的,但干燥过程会引起细胞应激并降低活性。冻干法经常被使用,但只有不到0.1%的细胞存活,这对于治疗用途来说是严重不足的。
保护策略,例如也可以添加糖类(如海藻糖和蔗糖)等辅料,但其保护机制仍不清楚,且效果因菌株而异。因此,目前没有有效的方法来保护厌氧菌免受严苛的加工应激和氧气暴露。
研究方法介绍
开发了一种新型的自组装涂层,用于保护有治疗价值的微生物,免受生产过程中的应激,包括氧气暴露和冻干。
涂层由金属-酚网络(metal-phenolic networks, MPNs)构成,这是金属离子与天然多酚,通过非共价配位形成的复合物。与依赖共价键的涂层不同,MPNs 通过非共价作用吸附在表面上。
先前的研究表明,MPNs 可以包覆哺乳动物细胞和酶,提供抵抗紫外线和裂解酶的保护。
然而,在此工作之前,MPNs 尚未应用于保护原核生物。我们用 MPNs 包覆大肠杆菌(Escherichia coli)和 Bacteroides thetaiotaomicron 的工作。
Bacteroides 属细菌对于肠道中的碳水化合物发酵至关重要。它们可以对抗危险的人侵微生物,并有潜力治疗结直肠癌。
我们开发了一种通用的方法来包覆微生物,对涂层进行了表征,并证明 MPNs 即使在缺乏典型冷冻保护剂的情况下,也能在冻干过程中保护生物治疗药物。
MPNs 是超分子网络,能够包覆多种基底。通过加入金属离子和多酚配位组分进行包封,过程快速、简便且生物相容性好,从而在目标表面形成 MPN 外壳。
使用 Fe(III) 离子和三种多酚之一:单宁酸(tannic acid, TA)、没食子酸(gallic acid, GA)或表没食子儿茶素没食子酸酯(epigallocatechin gallate, EGCG),成功地在大肠杆菌上形成了 MPNs(图1a,b)。
虽然许多金属离子可用于形成 MPNs,我们专注于 Fe(III),因为它成本低、被美国食品药品监督管理局(USFDA)认定为一般认为安全(generally recognized as safe, GRAS),且毒性低。
选择这三种多酚作为概念验证,因为它们同样被 USFDA 认定为 GRAS,是天然存在的,且相对便宜。
此外,这些多酚可用于螯合的酚羟基数量以及它们的分子直径彼此显著不同。因此我们预计这些分子能够代表可用的多酚范围。
在加入 MPN 组分并将 pH 调节至7.0-8.0后,无论是在空气中还是在氮气(N₂)气氛下,微生物悬液上都稳定地形成了 MPN 外壳(图S12)。
紫外-可见光谱中在500至600 nm之间出现配体-金属电荷转移(ligand-to-metal charge transfer, LMCT)吸收带,证实了稳定 MPN 复合物的形成(图1c和图S1)。
金属-酚膜通过成核随后自组装的方式在不同基底上形成。这个过程与基底的尺寸、形状和组成无关。因此,Fe(III)-TA 薄膜很容易在许多生物表面(包括真核生物和酵母)上形成,并且(如本文首次展示)也能在微生物上形成。
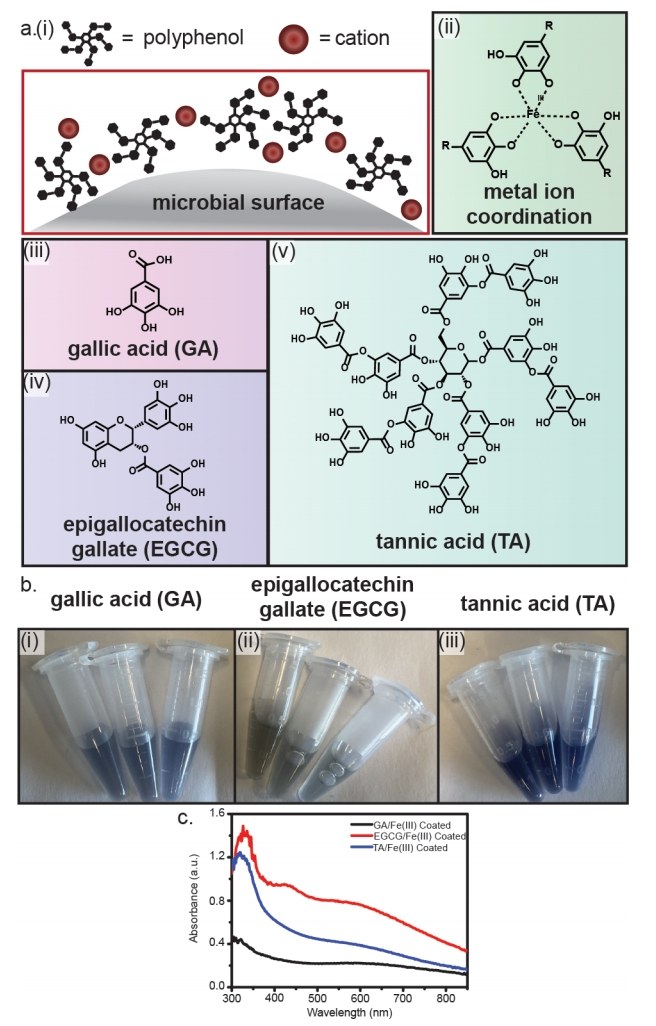
图1. 金属-酚网络(MPN)在微生物上的组装
(a) 细胞用多酚和金属离子的混合物包覆。评估了三种多酚:GA、EGCG和TA。
(b) 分别用(i) GA、(ii) EGCG或(iii) TA MPNs包覆的大肠杆菌。
(c) MPN包封大肠杆菌的紫外-可见光谱。
实验结果和数据分析
为了验证 MPN 外壳,确实形成于微生物表面,将荧光标记的蛋白质(牛血清白蛋白(BSA)-Alexa Fluor 647)与表达绿色荧光蛋白(GFP)的 MPN 包封大肠杆菌一起孵育。
BSA 优先吸附在 MPN 上,这可通过荧光显微镜观察到(图2a)。
对标记了 BSA-Alexa Fluor 647 的 MPN 包被大肠杆菌进行Z轴堆栈成像,进一步证实了核-壳结构(图S11)。
综合来看,成像结果证实了在每个微生物个体上形成了连续、均匀的外壳(图2a)。
扫描电子显微镜(SEM)图像进一步确认了 MPN 的组装,显示出单个大肠杆菌被包封在 Fe(III)-TA 复合物中,其粗糙的表面表明了这一点(图2b)。
未包被的大肠杆菌长度和宽度(分别为1.25 ± 0.29 μm 和 0.642 ± 0.044 μm)也比包被的细胞(分别为1.49 ± 0.25 μm 和 0.710 ± 0.060 μm)更短更窄,这可以解释为 MPN 在真空下保护了包被的微生物。
总之,这些结果证实了在单个微生物上成功形成了 MPNs,并且保持了天然的细胞形态。
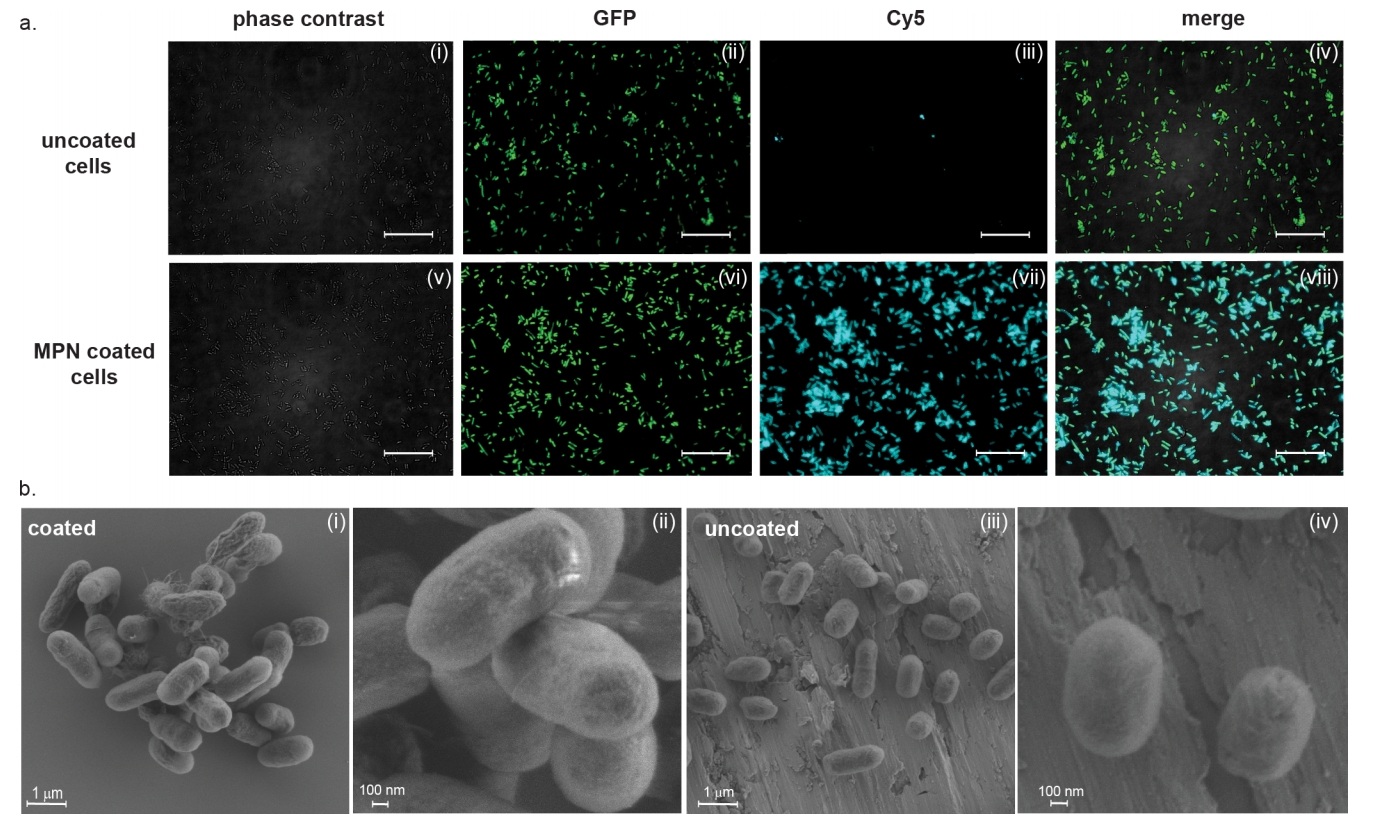
图2. 包封大肠杆菌的荧光和SEM图像
(a) 细胞用Alexa Fluor 647标记的BSA处理,该BSA会吸附到MPN上,但不会吸附到未包被的细胞上。
图中显示(i-iv)未包被和(v-viii)MPN包被的大肠杆菌(25922GFP)在相差通道、FITC通道(GFP)、Cy5通道(BSA-Alexa Fluor 647)的荧光图像以及合并图像。比例尺为20 μm。
(b) (i, ii) MPN包被和(iii, iv)未包被的大肠杆菌(MG1655)的SEM图像。比例尺:(i, iii) 1 μm, (ii, iv) 100 nm。
为了将 MPN 用作保护剂,细胞在包被后必须保持活性。
因此,我们通过测量600 nm处的光密度(OD₆₀₀)和菌落形成单位(colony forming unit, CFU)来监测细菌生长。
将连续稀释的包封大肠杆菌涂布在溶菌肉汤(lysogeny broth, LB)琼脂平板上或用于接种 LB 培养基,以未包被的细胞作为对照。
在37°C下培养48小时后,对平板上的菌落进行计数,并使用酶标仪连续监测大肠杆菌的 OD₆₀₀。
B. thetaiotaomicron 的 OD₆₀₀ 通过在氮气(N₂)气氛下使用酶标仪或在特定时间点于空气中进行评估。
天然大肠杆菌的 log(CFU/mL) 为8.41 ± 0.58,而 MPN 包封的大肠杆菌为5.00 ± 0.38,这表明在相同时间内包被细胞的分裂次数比未包被对照少3个数量级(图3a)。
有趣的是,仅用 FeCl₃ 或 TA 处理的细胞,其 log(CFU/mL) 值分别为9.80 ± 0.21或8.88 ± 0.40,略高于未包被细胞的值,这可能是由于添加了可溶性铁,铁是一种微量营养素,参与细菌生长。
这些结果表明,MPN 外壳在固体和液体培养基中均能抑制细胞分裂。
基于先前对真核生物的研究,已有研究表明 MPNs 可作为刚性屏障,阻止细胞在固体培养基中接触营养物质。
为了进一步探究,我们评估了用不同酚类(TA, GA 和 EGCG)形成的 MPNs, 对细胞分裂的抑制作用是否相同。
与未包被细胞相比,EGCG MPNs 使 CFU/mL 降低了100倍,GA MPNs 降低了10倍(图S2和S3),表明酚的结构对涂层的物理性质很重要。
在液体培养基中培养 MPN 包封的大肠杆菌也观察到类似的趋势,指数生长期延迟到包封后12.5小时(图3c)。
基于我们的假设(刚性影响细胞分裂延迟),我们同样预期涂层厚度会影响这种延迟。
不出所料,在厌氧条件下,MPN 包封的 B. thetaiotaomicron 的指数生长期延迟随着外壳厚度的增加而增加(图S4b)。
对于微生物生物治疗药物,细胞在给药时必须保持活性,因此分裂抑制是一个潜在的问题。
然而,细胞分裂抑制并不意味着细胞死亡,我们在包封后进行了荧光素二乙酸酯(fluorescein diacetate, FDA)检测以评估细胞活性。
FDA 是酯酶的底物,可用于测量酶活性和膜完整性。
我们观察到包封细胞有明显的荧光(图S5),证实了包被细胞是活的且具有代谢活性。
虽然我们的涂层不影响活性,但如果细胞无法分裂,其生长受到的影响可能会对生物治疗药物的递送构成挑战。
因此我们研究了 MPN 的解离。
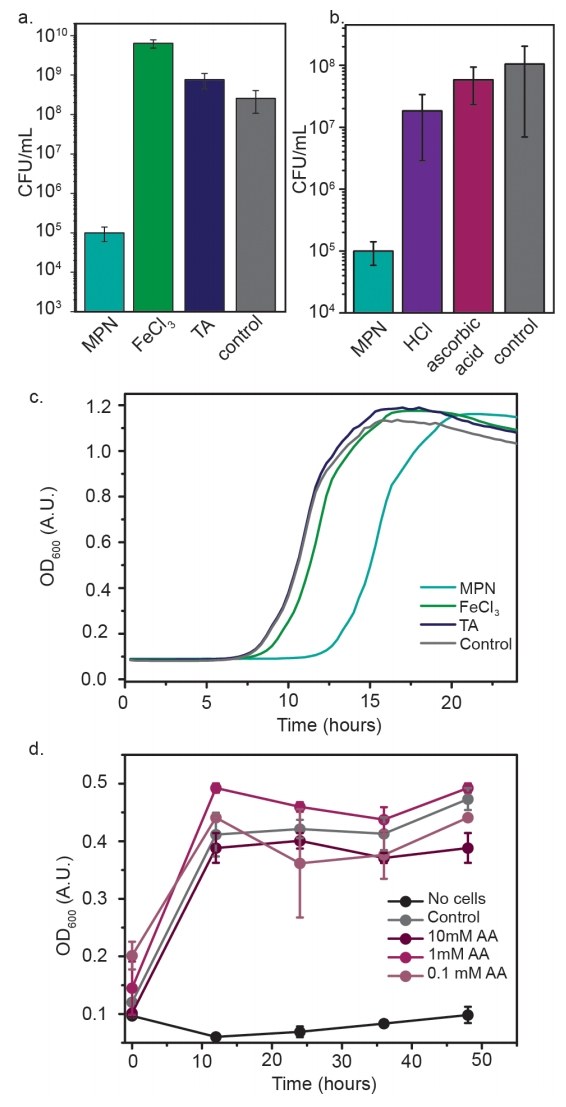
图3. 包封和解离后微生物的生长
(a) 包被大肠杆菌的CFU(蓝绿色:MPN包被;绿色:FeCl₃处理;蓝色:TA处理;灰色:未包被)。
(b) 酸处理后包被大肠杆菌的CFU(蓝绿色:MPN包被;紫色:MPN包被后用HCl处理;红色:MPN包被后用抗坏血酸(AA)处理;灰色:未包被)。
(c) 单独大肠杆菌、仅铁处理大肠杆菌、仅TA处理大肠杆菌和MPN包被大肠杆菌的生长曲线(基于OD₆₀₀)。虽然MPN包被细胞生长有延迟,但指数生长期的速率没有变化。
(d) 稀释AA处理(5分钟)后未包被 B. thetaiotaomicron 的生长曲线。误差线代表n=3个重复的标准差。
MPNs 对 pH 敏感,在用弱酸(类似于胃酸的条件)处理时容易降解,从而实现“按需”解离。
加入酸后,细胞悬液的颜色立即变为白色,表明 MPN 外壳被去除。在10 mM HCl 中孵育1小时后,包被大肠杆菌的 log(CFU/mL) 值增加到7.26 ± 1.07,指数生长期延迟(t_eg)减少到8小时,与未包被细胞相似(图3b)。
类似地,Fe(III)-TA 包封的 B. thetaiotaomicron 在用10 mM L-抗坏血酸(AA)处理仅5分钟后,t_eg 就减少到不足1小时(图S4a)。
使用较低浓度的 L-抗坏血酸 时,观察到 t_eg 恢复较慢(图S4a),而使用0.1 mM 酸处理则未观察到生长速率恢复。
重要的是,未包被 B. thetaiotaomicron 的生长速率不受这种酸处理的影响(图3d)。
用改良的禁食状态模拟胃液/肠液(FaSSGF/FaSSIF)处理时也观察到类似的趋势(图S13和S14)。
这些结果表明,MPN 外壳在与口服递送相关的条件下能够降解,因为包被产品在进入肠道之前会经过胃部(暴露于胃酸)。
因此,这种按需解离的特性适用于需要长期保存和体内控制释放的益生菌和生物治疗药物。
最后,我们确定了 MPN 涂层是否能在关键加工步骤——冻干过程中提供保护。
尽管冻干被广泛用于稳定治疗药物,但对于某些微生物,即使使用常见的冷冻保护剂,存活率也低于0.1%。
由于 MPNs 结构刚性,我们假设它们能在冻干过程中提供额外的保护。将包被细胞在不同缓冲液中速冻并冻干。在合适的液体培养基中复溶后监测 OD₆₀₀。
令人印象深刻的是,在添加了海藻糖的磷酸盐(PB)和磷酸柠檬酸(PC)缓冲液中,MPN 包被的大肠杆菌和 B. thetaiotaomicron 在孵育48小时后的 OD₆₀₀ 值均高于未包被的对照(图4a和图S6)。
值得注意的是,对于在不含冷冻保护剂的 PC 缓冲液中的包被大肠杆菌,48小时后观察到 OD₆₀₀ 增加了3倍(图4a)。
更显著的是,在类似条件下,B. thetaiotaomicron 在孵育96小时后进入指数期,而未包被的对照则没有观察到生长(图4b)。
这些改善表明,即使在缺乏常规冷冻保护剂的情况下,MPN 包被的微生物在冻干后也具有更高的存活率。
对于厌氧菌,Fe(III)-TA 提供了额外一层抵抗活性氧(reactive oxygen species, ROS)的保护,B. thetaiotaomicron 在氧气暴露后恢复更快,并且在 FeCl₃ 存在下冻干的两个菌株相比,未包被对照都显示出更高的 OD₆₀₀(图S7-S10)。MPN 包被的细胞在复溶后总是表现出最快的生长,这突显了 MPN 的保护能力。
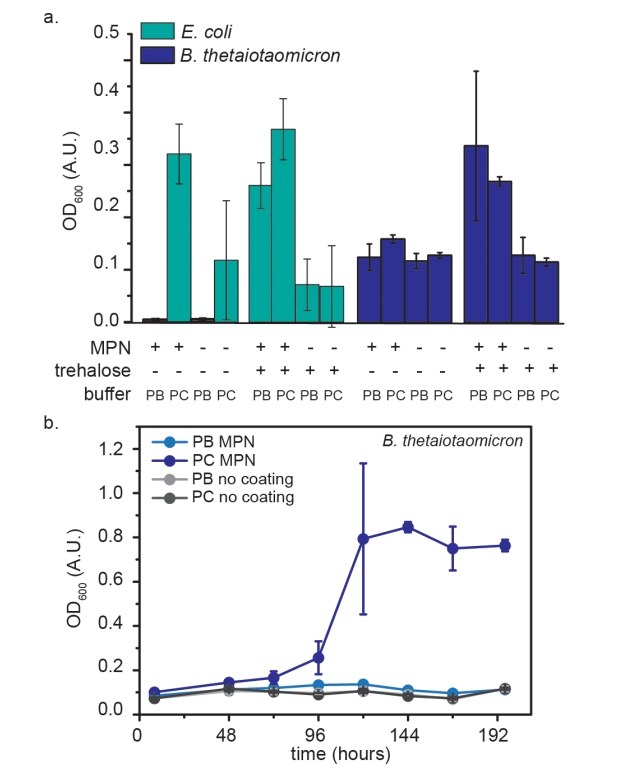
图4. MPN在冻干过程中对微生物的保护
(a) 冻干后的大肠杆菌和 B. thetaiotaomicron 在存在或不存在MPNs和冷冻保护剂的情况下生长48小时后的OD₆₀₀。
(b) B. thetaiotaomicron 在不含冷冻保护剂的条件下冻干后的生长曲线(PC:磷酸柠檬酸缓冲液;PB:磷酸盐缓冲盐水)。误差线代表n=3个重复的标准差。
总之,我们开发了一种用于微生物的自组装细胞涂层,以在加工过程中保持其活性。
这种简单的涂层由天然多酚和氯化铁组成,它们被美国 FDA 认定为 GRAS。
我们已经证明,这种生物相容性包封能够保护厌氧菌免受多种制造和储存应激(包括氧气暴露和冷冻干燥)的影响,且不需要添加剂(如冷冻保护剂或 ROS 清除剂)。
此外,该涂层在酸性条件下会迅速解离,这对于口服递送至肠道非常理想。
因此,我们解决了将微生物开发为活性生物治疗药物过程中的关键问题。
预计这种涂层策略可以扩展用于保护几乎任何细胞类生物治疗药物。
参考文献
《Protection of Anaerobic Microbes from Processing Stressors Using Metal–Phenolic Networks》 https://pubs.acs.org/doi/10.1021/jacs.1c09018?goto=articleMetrics&ref=pdf
相关产品
HZB325136:新型隐球酵母ATCC 32045(血清型:D) | Cryptococcus neoformans (Serotype:D)
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-04-30
编制人:小藻
审稿人:小藻
