益生菌的治疗潜力:它们在调节炎症中的作用
来源:武汉市灰藻生物科技有限公司 浏览量:40 发布时间:2026-04-27 14:55:29
摘要
益生菌(Probiotics)被世界卫生组织(WHO)定义为“摄入足够数量后对宿主产生健康益处的活微生物”。主要代表包括乳杆菌属(Lactobacillus)、双歧杆菌属(Bifidobacterium)以及布拉氏酵母(Saccharomyces boulardii)等。近年来,大量基础与临床研究证实,益生菌不仅可维持肠道微生态平衡,还能通过调节免疫应答、增强肠屏障功能、抑制促炎信号通路等方式系统性地缓解慢性炎症。
慢性低度炎症是2型糖尿病、动脉粥样硬化、肥胖、类风湿关节炎(RA)、炎症性肠病(IBD)、神经退行性疾病等多种复杂疾病的共同病理基础。益生菌通过多靶点、多通路干预这一过程,展现出作为辅助甚至一线治疗策略的巨大潜力。本文系统综述益生菌在炎症调控中的分子机制、临床证据、应用局限及未来发展方向,旨在为科研与临床实践提供参考。
一、引言
人类肠道内定植着约10¹⁴个微生物,其基因总量是人体自身基因组的150倍以上,构成复杂的“肠道微生物组”(gut microbiota)。这一生态系统与宿主免疫、代谢、神经功能紧密耦合。当菌群失衡(dysbiosis)发生时,有害菌过度增殖、有益菌减少,导致肠屏障破坏、内毒素(如脂多糖LPS)入血,激活全身性炎症反应。
益生菌正是通过重建这种平衡来发挥抗炎作用。目前全球已有数百种益生菌产品上市,涵盖食品、膳食补充剂及药品形式。然而,并非所有标称“益生菌”的产品都具备科学验证的健康功效——益生作用具有高度的菌株特异性(strain-specificity),即同一属的不同菌株可能效果迥异。
例如:
Lactobacillus rhamnosus GG(LGG)被广泛用于预防儿童抗生素相关性腹泻;
L. rhamnosus GR-1 则主要用于泌尿生殖道健康;
Bifidobacterium infantis 35624 在肠易激综合征(IBS)中显示出独特疗效。
因此,脱离具体菌株谈“益生菌”功效是不科学的。
二、益生菌如何调节免疫与炎症?
2.1增强肠道物理与免疫屏障
肠道上皮由单层细胞构成,细胞间通过紧密连接蛋白(如ZO-1、occludin、claudin-1)维持完整性。IBD、肥胖等疾病中,这些蛋白表达下降,导致“肠漏”(leaky gut),使细菌及其产物(如LPS)进入血液循环,触发系统性炎症。
多项动物与体外研究表明,益生菌(如 L. plantarum 299v、B. longum)可显著上调这些紧密连接蛋白的表达,修复肠屏障。例如,在DSS诱导的小鼠结肠炎模型中,给予 L. casei Zhang 后,ZO-1表达恢复,血清LPS水平下降40%以上。
2.2调控先天与适应性免疫应答
益生菌通过与肠上皮细胞和树突状细胞表面的模式识别受体(PRRs)互作,启动免疫调节:
TLR2/TLR10通路激活:诱导抗炎因子IL-10释放;
抑制TLR4/NF-κB通路:减少TNF-α、IL-6、IL-1β等促炎因子;
促进Treg细胞分化:通过分泌TGF-β或SCFAs,诱导Foxp3⁺调节性T细胞生成,抑制Th1/Th17过度活化。
一项针对健康志愿者的研究显示,连续4周服用含 L. acidophilus 和 B. bifidum 的复合益生菌后,外周血单核细胞中IL-10水平上升35%,而LPS刺激下的TNF-α反应降低28%。
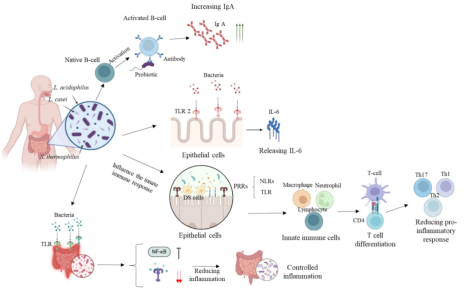
图1.益生菌与免疫调节
注:益生菌可通过激活B细胞,以剂量依赖的方式增强肠道免疫力,并促进免疫球蛋白A(IgA)的产生,这一效应在嗜酸乳杆菌(Lactobacillus acidophilus)、嗜热链球菌(Streptococcus thermophilus)和干酪乳杆菌(Lactobacillus casei)等菌株中尤为明显。此外,益生菌通过Toll样受体2(TLR2)通路刺激白细胞介素-6(IL-6)的释放,并与肠上皮细胞及树突状细胞表面的模式识别受体(PRRs)相互作用,促进调节性T细胞(Treg)的分化,同时抑制Th1、Th2和Th17介导的炎症反应。益生菌还能通过下调TLR表达并抑制核因子κB(NF-κB)信号通路,从而减少细胞因子的产生,有效缓解炎症。
2.3产生短链脂肪酸(SCFAs)——关键抗炎代谢物
益生菌(尤其是产丁酸菌如 Faecalibacterium prausnitzii、Roseburia spp.)发酵膳食纤维生成乙酸、丙酸和丁酸。其中,丁酸不仅是结肠上皮细胞的主要能量来源,还具有多重抗炎功能:
抑制组蛋白去乙酰化酶(HDAC),使染色质结构开放,促进抗炎基因转录;
阻断NF-κB核转位,降低IL-8、COX-2表达;
激活G蛋白偶联受体GPR43/GPR109A,诱导Treg扩增。
临床研究发现,IBD患者粪便中丁酸浓度显著低于健康人,而补充产丁酸益生菌或其前体(如抗性淀粉)可改善症状。
三、益生菌在具体炎症性疾病中的临床证据
3.1炎症性肠病(IBD)
溃疡性结肠炎(UC)
VSL#3(含4种乳杆菌、3种双歧杆菌、1种嗜热链球菌):在多项RCT中证实可诱导轻中度UC缓解。一项纳入124例患者的研究显示,VSL#3组缓解率达53%,显著高于安慰剂组(23%)。
大肠杆菌Nissle 1917:在维持UC缓解方面效果与美沙拉嗪相当,且耐受性更佳。
Bifidobacterium longum 536:在日本开展的试验中,连续8周服用可显著降低Mayo评分和粪便钙卫蛋白(炎症标志物)。
克罗恩病(CD)
目前证据较弱。两项小型RCT(共46例)显示,无论使用乳杆菌还是大肠杆菌Nissle 1917,均未能显著降低CD活动指数(CDAI)或诱导缓解(RR = 1.06, 95% CI: 0.65–1.71)。这可能与CD病变更深、涉及全层肠壁及Th1/Th17主导的免疫机制有关。
储袋炎(Pouchitis):VSL#3在术后预防复发方面效果突出。一项研究显示,12个月内85%的VSL#3使用者维持缓解,而安慰剂组仅6%。
3.2类风湿关节炎(RA)
2014年一项双盲RCT纳入46名女性RA患者,每日服用 L. casei 01(1×10⁸ CFU)8周。结果显示:
血清TNF-α下降32%,IL-6下降27%;
IL-10上升41%;
DAS-28(疾病活动评分)从4.8降至3.9(p<0.01)。
提示益生菌可通过调节Th17/Treg平衡改善自身免疫性炎症。
3.3代谢性炎症:肥胖与2型糖尿病
脂肪组织中的巨噬细胞浸润是胰岛素抵抗的关键驱动因素。研究发现:
肥胖者肠道中 Akkermansia muciniphila 丰度显著降低;
补充巴氏灭活的 A. muciniphila(10¹⁰ cells/天,3个月)可使胰岛素敏感性提高28%,血浆LPS下降24%,体重平均减少2.3 kg。
3.4神经炎症与精神健康(Psychobiotics)
肠-脑轴通过迷走神经、免疫因子、微生物代谢物三条通路双向沟通。益生菌干预可:
降低海马体小胶质细胞活化;
提高前额叶皮层GABA受体表达;
改善HPA轴应激反应。
临床试验显示:
L. rhamnosus JB-1 可降低小鼠焦虑行为,并改变GABA受体分布;
B. longum 1714 在健康志愿者中显著降低压力感知和皮质醇水平;
多菌株益生菌(含 L. helveticus R0052 + B. longum R0175)在6周内显著改善抑郁量表(HADS)评分。
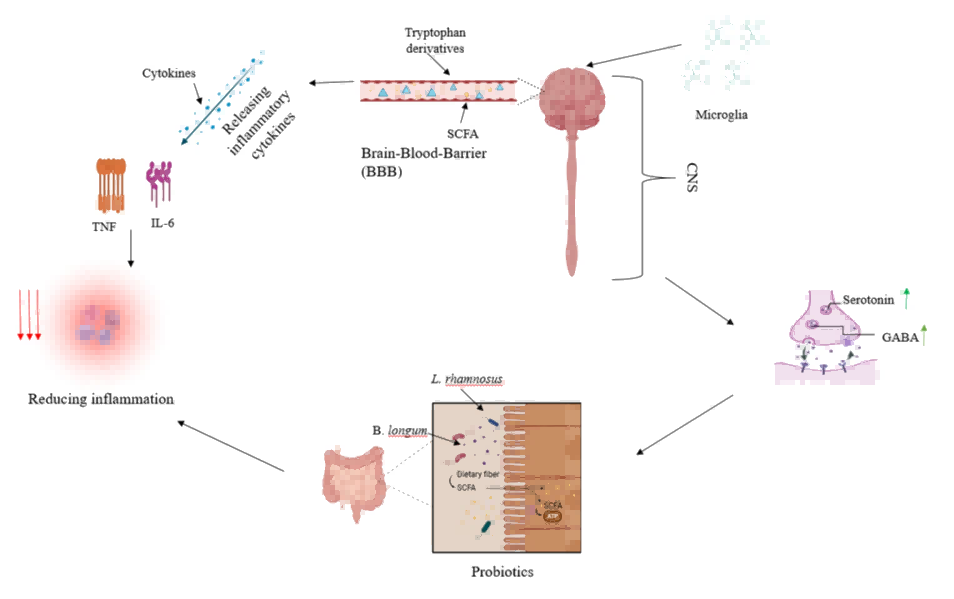
图2.肠-脑轴:微生物代谢物与神经炎症
注:SCFA:短链脂肪酸;GABA:γ-氨基丁酸;TNF:肿瘤坏死因子;IL-6:白细胞介素-6;CNS:中枢神经系统。
四、益生菌与传统抗炎药物:机制与疗效比较
4.1.益生菌的抗炎机制
多项体外研究(如HT-29肠上皮细胞模型)表明,乳杆菌和双歧杆菌组成的益生菌混合物可通过多种途径抑制炎症:
调控关键信号通路:显著抑制NF-κB和JAK/STAT通路中多个基因(如STAT1–6、JAK1–3、NEMO、TIRAP、RIP)的表达;
降低促炎因子:减少IL-6、IL-1β等细胞因子的释放;
修复肠道屏障:上调紧密连接蛋白(ZO-1、claudin-1、occludin)表达,改善“肠漏”;
竞争与代谢作用:与致病菌争夺生态位、分泌抗菌物质,并产生具有抗炎活性的短链脂肪酸(SCFAs)。
值得注意的是,在炎症已启动后给药(PLB模式)的抑制效果最强,甚至可将STAT6等基因表达降至接近零,说明益生菌不仅有预防作用,还具备治疗潜力。
此外,某些益生菌(如脆弱拟杆菌)的代谢产物或培养上清液本身即可诱导调节性T细胞(Treg)、改善肠道通透性并抑制炎症。
表1.益生菌抗炎作用的总结
| 力益生菌菌株 | 研究对象/靶点 | 样本量 | 研究周期 | 主要结果 |
|---|---|---|---|---|
| L. casei Shirota | 人类树突状细胞(DC) | - | - | 来自溃疡性结肠炎(UC)患者样本的树突状细胞表现出IL-22和干扰素-γ(IFN-γ)分泌增加、IL-4分泌减少。L. casei Shirota处理可通过降低TLR2和TLR4表达,恢复其正常的免疫刺激能力。 |
| L. plantarum 菌株 CGMCC1258 | IPEC-J2细胞模型 | - | - | L. plantarum 治疗可降低IL-8、TNF及TLRs负调控因子的转录丰度;同时抑制闭合蛋白(occludin)的基因和蛋白表达。 |
| L. delbrueckii subsp. delbrueckii TUA4408L | PIE细胞 | - | - | 由鼠伤寒沙门氏菌(E. coli 987P)诱导的MAPK和NFκB通路激活,可通过上调TLR负调控因子(主要为TLR2)而被下调。 |
| E. coli Nissle 1917 和 L. rhamnosus GG | IEC 6细胞 | - | - | 预先使用这些益生菌可预防或抑制由5-FU诱导的肠上皮细胞凋亡以及肠道屏障功能丧失。 |
| L. paracasei CNCM I 4034, B. breve CNCM I 4035, L. rhamnosus CNCM I 4036 | 树突状细胞(DC) | - | - | 诱导TLR9表达和TGF-β分泌;培养上清液(CFS)处理可降低促炎细胞因子和趋化因子水平。 |
| B. longum 536 | 中轻度UC患者 | 56例 | 8周 | 益生菌给药改善了中轻度至中度活动性UC患者的临床症状。 |
| S. faecalis, C. butyricum, B. mesentericus | UC缓解期门诊患者 | 60例 | 12个月 | 益生菌在维持UC患者临床缓解方面有效。 |
| L. plantarum 299v | 中轻度UC患者 | 74例 | 8周 | 益生菌补充安全、耐受性良好、口感佳,能有效降低中轻度UC患者的疾病活动评分。 |
| E. coli Nissle 1917 | UC患者 | 100例 | 7周 | 在活动性UC患者中,E. coli Nissle 1917作为常规治疗的附加疗法无额外益处。 |
| 含双歧杆菌、乳酸杆菌和Streptococcus thermophilus的胶囊 | 回肠造口术后患者(CD) | 119例 | 90天 | 益生菌组与安慰剂组在内镜复发率上无差异,但黏膜层的炎症细胞因子(IL-8、IL-1)水平在益生菌组更低。 |
| L. casei subsp. rhamnosus GG | 健康个体、CD患者、UC患者 | 50名健康人、37名CD患者、15名UC患者 | 90天 | 对抗细胞壁水解酶的IgA抗体水平在L. casei subsp. rhamnosus GG组显著更高。 |
| L. acidophilus LA 5, L. delbrueckii subsp. bulgaricus LBY-27, B. animalis subsp. lactis BB 12, S. thermophilus STY 31 | CD和UC患者 | 8名CD患者、8名UC患者 | 1个月 | CD与UC患者肠道微生物组成无显著差异,且细菌谱未因益生菌干预而改变。 |
| L. acidophilus Ecologic 825, B. bifidum (W23), B. lactis (W51), B. lactis (W52), L. acidophilus (W22), L. casei (W56), L. paracasei (W20), L. plantarum (W62), L. salivarius (W24), L. lactis (W19) | 慢性储袋炎患者 | 16例慢性储袋炎患者 + 13名对照者 | 8周 | 益生菌恢复了储袋炎患者对大肠杆菌的黏膜屏障功能。 |
| B. infantis 35,624 | UC、慢性疲劳综合征、银屑病患者 | 22名UC患者、48名慢性疲劳综合征患者、26名银屑病患者 | 6–8周 | 益生菌显著降低了胃肠道和非胃肠道疾病患者系统性促炎生物标志物水平。 |
| S. boulardii | 克罗恩病(CD) | 165例CD患者 | 52周 | 益生菌耐受性良好但无明显疗效;治疗期间共发生21例不良事件(AEs),其中17例在S. boulardii组,8例在安慰剂组。 |
| Escherichia coli Nissle 1917 和某些乳杆菌菌株 | 克罗恩病(CD) | 46名德国和英国公民(轻至重度炎症症状) | 6个月 | 在活动性克罗恩病患者中,益生菌治疗无显著获益。 |
| Lactobacillus GG, Enterobacteriaceae, Clostridiales | 非酒精性脂肪性肝病(NAFLD) | 36例 | 12周 | 治疗后肝硬化伴轻微肝性脑病患者炎症减轻,认知功能改善。 |
| Lactobacillus casei 01 | 类风湿关节炎(RA) | 46名女性患者 | 8周 | 显著降低炎症水平并改善疾病活动评分。 |
| VSL#3 | 复发性或难治性储袋炎 | 36例 | 12个月 | 高剂量VSL#3可有效维持复发性或难治性储袋炎患者的缓解状态。 |
| Limosilactobacillus fermentum 菌株 | 饮食对肠道菌群及系统性炎症的影响 | - | - | 研究强调了L. fermentum在改善肠道健康、发挥抗炎和免疫调节作用方面的有益特性。 |
| Bacillus subtilis DE111 | 功能特性、安全性及改善消化与免疫健康的潜力 | - | - | 突显其通过增强酶产生和抗氧化活性来促进消化和免疫健康的潜力,适用于功能性食品开发。 |
| Ligilactobacillus salivarius P1 CEA3 | 安全性和益生特性评估 | - | - | 基于基因组分析,该菌株具有作为益生菌或天然抗菌剂在动物和人类健康中应用的巨大潜。 |
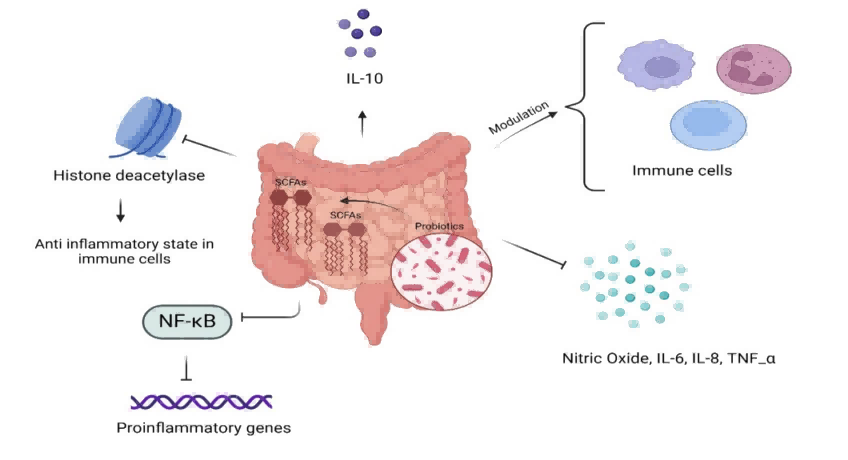
图3.益生菌与短链脂肪酸(SCFAs)在肠道健康中的作用
注:益生菌(如乳酸菌和大肠杆菌KUB-36)通过发酵碳水化合物产生短链脂肪酸(SCFAs),包括丁酸、乙酸和丙酸,从而调节免疫反应、减轻炎症,维持肠道健康。
4.2.与传统药物的对比
部分新型策略(如清除活性氧ROS、激活Nrf2抗氧化通路)也正在拓展抗炎治疗边界,但益生菌因其天然、低毒、多效的特点,在慢性病长期管理中更具优势。
表2.益生菌与传统抗炎药物的比较
| 维度 | 传统抗炎药物(5-ASA、激素、生物制剂等) | 益生菌 |
|---|---|---|
| 作用靶点 | 直接阻断特定分子(如TNF-α、IL-6、JAK) | 多靶点协同:通路抑制 + 屏障修复 + 菌群调节 + 代谢物生成 |
| 作用范围 | 全身性,常伴免疫抑制、感染风险等副作用 | 主要作用于肠道,安全性高,耐受性好 |
| 治疗目标 | 控制症状、诱导缓解 | 重建肠道稳态,预防复发 |
| 核心共性 | 均以“调节异常免疫与炎症”为核心目标 | 均以“调节异常免疫与炎症”为核心目标 |
4.3.临床应用需“精准选择”
益生菌并非“万能”,其效果高度依赖菌株、疾病类型和个体差异:
有效场景:
溃疡性结肠炎(UC):VSL#3、大肠杆菌Nissle 1917、长双歧杆菌536、植物乳杆菌299v等可减轻症状、维持缓解;
储袋炎:VSL#3是目前证据最充分的益生菌疗法;
辅助治疗:联合常规药物可减少副作用、提升生活质量。
效果有限或无效:
克罗恩病(CD):多数益生菌(包括LGG、LA1)未能显著降低复发率;
部分研究中,益生菌对IBD整体疗效不一致,提示需个体化选择。
此外,益生菌在哮喘、过敏、糖尿病甚至新冠等非肠道炎症性疾病中也显示出潜在价值,可能通过肠-全身轴调节免疫耐受。
4.4.未来方向
开展大样本、多中心随机对照试验(RCTs),明确不同菌株的适应症;
推动“菌株特异性”理念,避免笼统宣称“益生菌有效”;
加强医生和公众教育,提升对益生菌科学使用的认知;
探索益生菌与药物、益生元、饮食的整合治疗方案。
五、影响益生菌疗效的关键变量
5.1菌株特异性
L. reuteri DSM 17938:有效缓解婴儿绞痛;
L. reuteri ATCC PTA 6475:可抑制乳腺癌细胞增殖;
同一菌种不同亚型功能差异巨大。
5.2剂量与给药方式
CFU(菌落形成单位)是衡量剂量的核心指标:
- 抗生素相关性腹泻:≥10¹⁰ CFU/天;
- IBS:5×10⁹ – 10¹⁰ CFU/天;
- 早产儿:每菌株约 10⁹ CFU 即可有效定植。
给药时机:炎症发生后给药(PLB模式)在体外模型中反而抑制效果最强,提示其具备“治疗窗口”。
5.3个体基线菌群状态
研究发现,约30–50%人群属于“益生菌抵抗型”(probiotic-resistant),其肠道原有菌群会排斥外源益生菌定植。这类人群可能更适合接受自体粪菌移植(autologous FMT)或合生元(益生菌+益生元)方案。
5.4制剂技术
普通冻干粉在胃酸中存活率不足10%。采用微胶囊包埋、藻酸盐涂层或乳制品基质(如酸奶)可将存活率提升至50%以上,显著增强疗效。
六、下一代益生菌(NGPs):迈向精准微生物疗法
传统益生菌多源于食品发酵,功能有限。而下一代益生菌(Next-Generation Probiotics, NGPs)是从人体分离的共生菌或条件致病菌改造体,具有明确治疗靶点:
6.1代表性NGPs:
Akkermansia muciniphila:降血糖、减重、抗炎,已进入II期临床;
Faecalibacterium prausnitzii:IBD患者中显著缺失,其培养上清液可抑制NF-κB;
E. coli Nissle 1917 工程菌:可感应肠道炎症并释放IL-10或抗氧化酶。
6.2工程化策略:
利用CRISPR-Cas9敲入治疗基因;
构建“炎症感应-药物释放”闭环系统;
开发结肠靶向微粒递送系统,避免胃酸破坏。
例如,Huang等人构建的工程 E. coli Nissle 可在肿瘤缺氧区表达过氧化氢酶,分解H₂O₂,缓解缺氧并增强放疗效果(Sci Transl Med, 2020)。
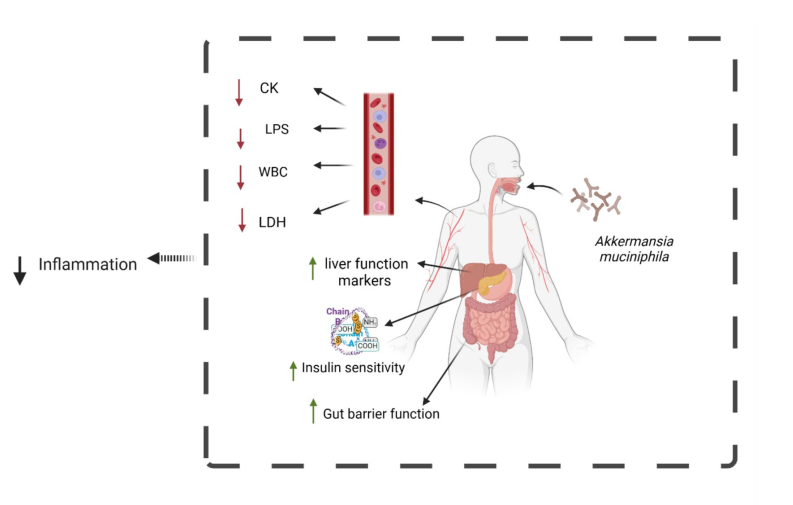
图4.嗜黏蛋白阿克曼菌(Akkermansia muciniphila)的抗炎机制
注:CK:肌酸激酶;LPS:脂多糖;WBC:白细胞;LDH:乳酸脱氢酶。
七、当前研究局限与未来方向
7.1主要局限:
1. 样本量小:多数RCT < 100人,统计效力不足;
2. 菌株混杂:不同研究使用不同菌株,难以横向比较;
3. 随访时间短:缺乏长期安全性与疗效数据;
4. 机制不清:多数研究停留在表型观察,缺乏分子通路验证。
7.2未来重点方向:
1. 机制深挖:利用单细胞测序、代谢组学、类器官模型解析益生菌-宿主互作;
2. 个性化干预:基于宏基因组分型(enterotype)选择最优菌株;
3. 合生元优化:筛选能促进特定益生菌定植的益生元(如低聚果糖、抗性淀粉);
4. 监管标准化:建立益生菌功效评价的国际标准(如EFSA、FDA的健康声称审批流程);
5. 拓展适应症:探索在阿尔茨海默病、帕金森病、抑郁症、癌症免疫治疗中的辅助作用。
八、结论
益生菌已从传统“肠道保健”概念跃升为调控全身炎症网络的重要工具。其通过修复屏障、重塑菌群、调节免疫、生成代谢物等多维机制,在IBD、RA、代谢综合征、神经精神疾病等领域展现出独特优势。
然而,必须清醒认识到:益生菌不是“万能神药”。其疗效高度依赖于菌株选择、剂量设计、个体特征和疾病阶段。盲目使用不仅无效,还可能干扰原有菌群平衡。
未来,随着合成生物学、人工智能(如菌群-宿主互作预测模型)和精准医学的发展,益生菌将从“经验性补充”走向“靶向性治疗”,成为慢性炎症性疾病综合管理中不可或缺的一环。在此过程中,加强医生教育、规范产品标识、推动高质量临床研究,是实现其治疗潜力的关键前提。
参考文献
1.Mazziotta C et al (2023) Probiotics mechanism of action on immune cells and beneficial effects on human health. Cells 12(1):184
2.Javanshir N et al (2025) The antiviral effects and underlying mechanisms of probiotics on viral infections. Microb Pathogen 12:107377
3.Zheng Y et al (2023) Probiotics fortify intestinal barrier function: a systematic review and meta-analysis of randomized trials. Front Immunol 14:1143548
4.Kang C-H et al (2021) Antioxidant activity and short-chain fatty acid production of lactic acid bacteria isolated from Korean individuals and fermented foods. 3 Biotech 11(5):217
5.Chakraborty J (2023) Microbiota and the plant immune system work together to defend against pathogens. Arch Microbiol 205(10):347
6.Rahkola E-N et al (2023) The preterm gut microbiota and administration routes of different probiotics: a randomized controlled trial. Pediatr Res 94(4):1480–1487
相关产品
HZB196543:植物乳杆菌 | Lactobacillus plantarum
HZB357487:德氏乳杆菌保加利亚亚种| Lactobacillus delbrueckii subsp. bulgaricus
HZB205362:布拉酵母菌 | Saccharomyces Boulardii
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-04-23
编制人:思琪
审稿人:小藻
