专性厌氧菌的“生命禁区”:氧毒性机制与极限厌氧培养技术解析
来源:武汉市灰藻生物科技有限公司 浏览量:166 发布时间:2026-04-01 12:33:19
一、引言
在地球演化史的最初二十亿年里,生命完全在没有氧气的环境中孕育与繁衍。
尽管氧气(O₂)已成为大多数生物维持生命活动的必需底物,但在人类的肠道深处、深海热泉以及发酵工业的反应器中,依然潜伏着一个庞大而神秘的群落——厌氧微生物(Anaerobic Microorganisms)。
对于其中的专性厌氧菌(Obligate Anaerobes)而言,氧气非但不是能量代谢的动力,反而是一种剧毒的化学试剂。微量的氧气暴露,就足以在几分钟内彻底摧毁它们的代谢酶系与遗传物质。
随着肠道微生态学(Microbiome)、活体生物药(LBP)以及高价值挥发性脂肪酸(VFAs)发酵工程的迅速崛起,如何在体外实验室环境中完美复刻无氧的“生命禁区”,成为了生物科技领域不可回避的核心挑战。
本文将从氧毒性的生化本质出发,深度解析氧化还原电位(ORP)的热力学调控机制,并带您领略极限厌氧培养的工程学艺术。
二、氧毒性的生化本质:ROS风暴与酶系统的“裸奔”
为什么氧气会对专性厌氧菌造成致命打击?答案隐藏在细胞内部的电子传递过程与抗氧化酶防线的天然缺失中。
2.1 活性氧(ROS)的无差别攻击
在正常的厌氧代谢中,电子应当被精确传递给特定的终端受体(如硫酸盐、硝酸盐或二氧化碳)。
然而,当环境中存在氧气时,O₂ 极强的电负性会强行从厌氧菌的黄素蛋白或铁氧还蛋白中“抢夺”单电子,从而生成极其活泼的活性氧自由基(Reactive Oxygen Species, ROS)
其主要包括超氧阴离子(O₂·⁻)、过氧化氢(H₂O₂)和羟基自由基(·OH)。
这些 ROS 具有强烈的氧化性,它们会无差别地攻击细胞膜引发脂质过氧化、破坏蛋白质的三维构象,并直接切断 DNA 双链,导致细胞发生不可逆的生理损伤与凋亡。
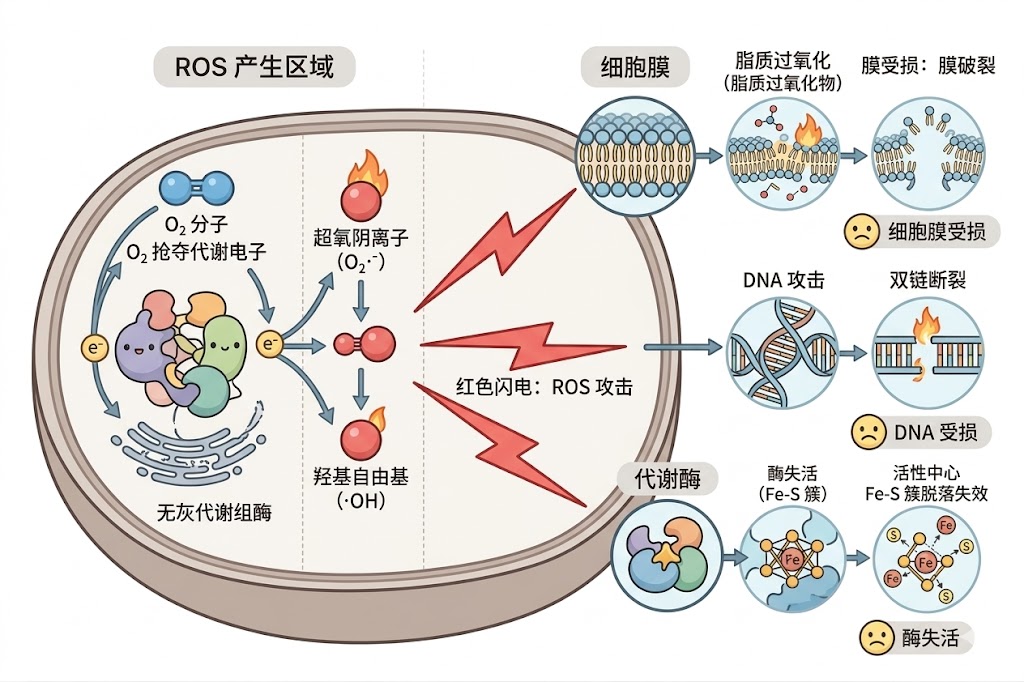
图1. 氧气诱导的 ROS 生成及其对专性厌氧菌生物大分子的破坏作用
2.2 抗氧化酶防线的天然缺失
好氧生物之所以能在高氧环境中生存,是因为它们在漫长的进化中获得了一套强大的“灭火系统”:超氧化物歧化酶(SOD)
这套系统能将超氧阴离子转化为过氧化氢,而过氧化氢酶(Catalase)和过氧化物酶(Peroxidase)则进一步将其分解为无害的水和氧气。
然而,绝大多数专性厌氧菌(如梭菌属、双歧杆菌属)的基因组中,天然缺失编码这些抗氧化酶的基因。这意味着它们在氧气面前处于完全“裸奔”的状态,没有任何抵御 ROS 的生化屏障。
三、不仅要“无氧”,更要“低电位”:氧化还原电位(Eh)的奥秘
在厌氧培养的实际操作中,研究人员最常犯的错误之一是认为“抽真空通入高纯氮气”就万事大吉了。然而,真正决定专性厌氧菌能否生长的核心生化指标,是培养基的氧化还原电位(ORP,通常用 Eh 表示)。
3.1 Eh 值与细胞代谢的热力学限制
Eh 值反映了环境中电子供体与电子受体的相对比例。正值代表体系处于氧化态,负值代表处于还原态。
一般的需氧菌在 Eh 值为 +300 mV 到 +400 mV 的环境中生长良好;而专性厌氧菌的代谢反应(如产甲烷、硫酸盐还原)在热力学上必须依赖极低的还原电位才能自发进行。
例如,普通的脆弱拟杆菌(Bacteroides fragilis)需要环境 Eh 低于 -250 mV 才能开始细胞分裂;而极度严苛的产甲烷古菌,甚至要求 Eh 降低至 -330 mV 以下。
如果仅仅依靠物理除氧(如通气置换),培养基的 Eh 值通常只能降至 +100 mV 左右,远远达不到绝大多数厌氧菌繁衍的“阈值”。
| 微生物耐氧等级分类 | 代表性菌株 | 抗氧化酶系统配置 | 生长所需的最高 Eh 阈值 |
|---|---|---|---|
| 专性好氧菌 (Obligate Aerobe) | 枯草芽孢杆菌 (B. subtilis) | 含丰富 SOD 与 Catalase | +300 mV 至 +400 mV |
| 兼性厌氧菌 (Facultative Anaerobe) | 大肠杆菌 (E. coli) | 含 SOD 与 Catalase | 宽泛,-200 mV 至 +300 mV 均可 |
| 耐氧厌氧菌 (Aerotolerant Anaerobe) | 植物乳杆菌 (L. plantarum) | 仅含少量 SOD 或替代型过氧化物酶 | 0 mV 至 +100 mV |
| 专性厌氧菌 (Obligate Anaerobe) | 生孢梭菌 (C. sporogenes) | 完全缺失 SOD 与 Catalase | < -200 mV |
四、极限厌氧培养基的配制艺术:还原剂与指示剂的交响
为了强行将培养基的 Eh 值拉低至“生命禁区”的水平,并在整个实验或发酵周期内维持绝对的还原态,我们在配制厌氧培养基时必须引入化学还原剂与氧化还原指示剂这两大核心组分。
4.1 强效化学还原剂(Reducing Agents)
常用的还原剂通过消耗体系内的残余微量氧气,并释放电子来大幅度降低环境电位。
不同强度的还原剂适用于不同严苛程度的目标菌株:
巯基乙酸钠(Sodium Thioglycolate)常用于温和厌氧菌和药典规定的无菌检查培养基(如 FTM);
L-半胱氨酸盐酸盐(L-Cysteine HCl)是目前厌氧实验室中最常用的强效还原剂,它含有活泼的巯基(-SH),能够迅速将培养基的 Eh 值降至 -200 mV 以下;
硫化钠(Na₂S)具有极强的还原性,能将 Eh 降至 -300 mV 级别,常用于最苛刻的专性厌氧古菌培养,但在配置时需要极高的安全操作技巧。
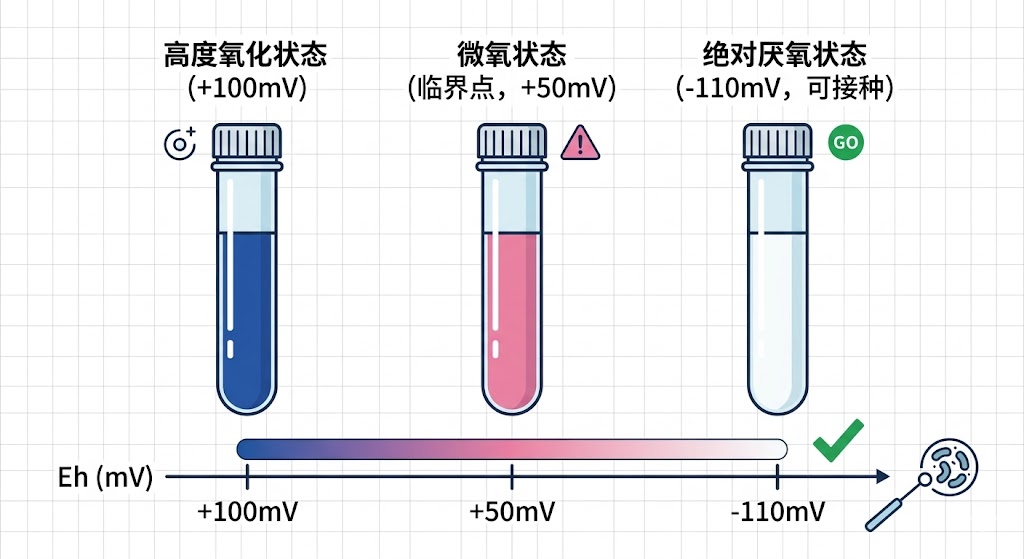
图2. 刃天青(Resazurin):厌氧实验的指示剂
4.2 氧化还原指示剂:刃天青(Resazurin)
如何直观地判断肉眼不可见的氧气是否已经彻底耗尽?
刃天青(Resazurin)无疑是厌氧学家的“眼睛”。
这种独特的染料在高度氧化时呈深蓝色;在 Eh 降至 +50 mV 左右时变为粉红色;当体系彻底进入厌氧还原状态(Eh < -110 mV)时,则会被还原为无色的氢化试卤灵(Resorufin)。
在任何分离或培养环节,若是看到培养基泛起一抹粉红,即宣告厌氧屏障已被击穿,实验必须立即停止并重新排查泄露点。
五、厌氧操作的工程学屏障:从亨盖特滚管到厌氧手套箱
要实现从菌株复苏、接种、培养到代谢物取样的全流程隔绝氧气,单靠化学试剂的保护是远远不够的,必须借助严密的工程学设备来搭建物理屏障。
5.1 亨盖特(Hungate)厌氧滚管技术
由厌氧微生物学先驱 Robert Hungate 发明的滚管技术,至今仍是分离极端厌氧菌的经典方案。
该技术不依赖庞大的厌氧箱,而是使用坚固的螺口厌氧管。在持续通入无氧高纯气流(如 N₂ 或 CO₂)的保护下,进行液体接种和固体融化涂布。
管内的顶空气体在封口瞬间被完全置换,使每一支试管都成为一个独立的微型厌氧反应器,确保了单菌落分离的可靠性。
5.2 催化循环与厌氧操作台(Anaerobic Chamber)
现代微生物实验室为了提高通量,普遍采用大型的厌氧手套箱。
除了通过反复抽真空与充气来置换过渡舱(Airlock)的气体外,箱体维持绝对无氧的核心秘密在于钯(Palladium, Pd)催化剂与混合工作气体(通常为 85% N₂, 10% H₂, 5% CO₂)的配合。
在常温下,箱内循环风机不断将气体吹过含有钯颗粒的网包。钯作为高效催化剂,能促使工作气体中的氢气(H₂)与任何不慎渗入箱内的微量氧气(O₂)发生剧烈反应生成水(2H₂ + O₂ → 2H₂O),从而将箱体内的氧浓度压制在 5 ppm 以下的安全水平。
六、结语
剥开自然界好氧生态的表象,厌氧微生物群落才是地球物质循环的底层密码,更是人类健康与发酵工程未被完全挖掘的巨大宝库。
从深刻理解 ROS 的破坏力,到精准驾驭氧化还原电位(ORP);从半胱氨酸的巯基还原,到钯催化除氧的精密循环,专性厌氧菌的培养不仅是一门严谨的生物科学,更是一门充满细节挑战的实验艺术。
作为专业的生物保藏与资源提供方,我们深知每一株厌氧模式菌的脆弱与珍贵。只有在源头把控极低电位的复苏工艺,严守耗材的无氧屏障,才能确保您手中的每一管标准菌株,都能在您的实验台上重现其最为强悍的代谢活力。
参考文献
1. Hungate, R. E. (1969). A roll tube method for cultivation of strict anaerobes. Methods in Microbiology, 3, 117-132.
2. Morris, J. G. (1975). The physiology of obligate anaerobiosis. Advances in Microbial Physiology, 12, 169-246.
3. Imlay, J. A. (2019). Where in the world do bacteria experience oxidative stress?. Environmental Microbiology, 21(2), 521-530.
相关技术与支撑体系
HZB356023: Eubacterium coprostanoligenes Freier et al.
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-03-31
编制人:小段
审稿人:小藻
