让生命显色:自标记蛋白标签的灵活性与应用
来源:武汉市灰藻生物科技有限公司 浏览量:91 发布时间:2026-03-28 20:46:45
引言:告别“质粒囤积”困境
审视典型的实验室超低温冰箱,您往往会发现一种普遍现象:针对同一目标蛋白,研究者构建了繁多的质粒变体。
这些质粒分别融合了,绿色荧光蛋白(GFP)、红色荧光蛋白(RFP)、新型荧光变体、亲和纯化标签,甚至是重复构建的相同荧光蛋白版本,往往源于对既有库存的遗忘。
这种“一蛋白一质粒”的模式不仅造成了资源浪费,更限制了实验设计的灵活性。
倘若存在一种通用融合蛋白策略,能够根据实验需求随意切换荧光颜色或功能标签,那将如何改变研究格局?
这并非科幻构想,而是已成现实的自标记蛋白标签(Self-Labeling Protein Tags)技术。本文将深入探讨该技术的核心原理、主流工具及其在前沿生物研究中的多样化应用。
一、核心原理:酶促共价标记的化学魔法
自标记蛋白标签的本质,是一类经过工程化改造的酶。这些酶通常通过突变丧失了原有的催化活性,但保留了与特定底物形成共价键的能力。
其工作流程极为简洁高效:
基因融合:将编码自标记标签的序列与目标蛋白基因融合,表达出融合蛋白。
配体孵育:向体系中加入带有特定功能基团(如荧光染料、生物素等)的底物配体。
特异性结合:标签酶识别并共价捕获配体,从而将功能分子精准锚定在目标蛋白上。
这一策略赋予了研究者前所未有的灵活性:无需反复进行繁琐的分子克隆,仅需更换不同的化学配体,即可在同一融合蛋白上实现多色成像、超分辨率追踪或多功能修饰。
此外,有机染料在光物理特性(如亮度、光稳定性)上显著优于传统荧光蛋白,极大地拓展了显微成像的应用边界。
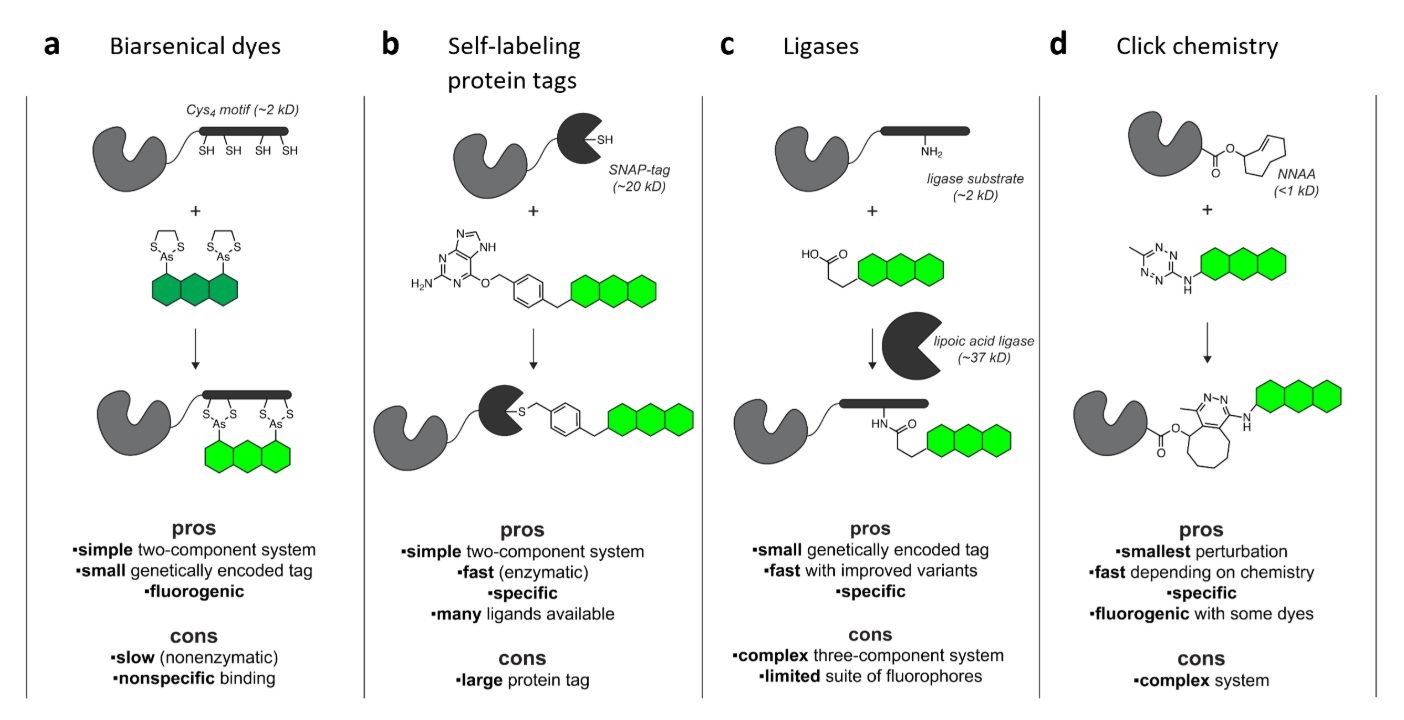
图1:活细胞标记策略。绿色结构代表荧光团或其他有用的配体,灰色结构是关注的蛋白质,黑色是融合标记或标记系统。图片改编自Lavis,2016年,CC-BY。
二、主流自标记标签系统
自该技术问世以来,多种基于不同酶学机制的标签系统相继开发,各具特色:
1、四半胱氨酸标签(Tetracysteine Tag, FlAsH/ReAsH)
起源:1998年由Roger Tsien实验室首次报道(Griffin et al., 1998)。
结构:仅由15个氨基酸组成的短肽序列(基序为CCXXCC,X为非半胱氨酸氨基酸)。
机制:特异性结合双砷染料,如绿色的FlAsH(荧光素衍生物)或红色的ReAsH(试卤灵衍生物)。
优势:体积极小,对目标蛋白功能干扰最小。
2、SNAP-tag
起源:2003年由Kai Johnsson实验室开发(Keppler et al., 2003)。
结构:基于人源DNA修复蛋白O⁶-烷基鸟嘌呤-DNA烷基转移酶(hAGT)的工程化变体。
机制:与O⁶-苄基鸟嘌呤(BG)衍生物配体发生不可逆的共价结合。
变体:后续开发了反应动力学更快的SNAPf版本。
3、eDHFR 标签
起源:2005年由Virginia Cornish和Michael Hecht实验室证实(Miller et al., 2005)。
结构:大肠杆菌二氢叶酸还原酶(eDHFR)。
机制:最初利用其与三甲氧苄二氨基嘧啶(TMP)衍生物的高亲和力非共价结合;后经引入Leu28Cys突变(Gallagher et al., 2009),实现了与TMP配体的共价连接。
4、HaloTag
起源:2008年由Promega公司研发(Los et al., 2008),目前已成为Addgene等平台最受欢迎的自标记标签。
结构:基于细菌卤代烷烃脱卤素酶的工程化变体(标准版为HaloTag7,最新变体已迭代至HaloTag11)。
机制:特异性结合合成氯烷烃(CA)配体,形成稳定的共价键。
5、CLIP-tag
起源:2008年同样由Kai Johnsson实验室推出(Gautier et al., 2008)。
结构:同样基于hAGT酶,但经过不同位点的突变改造。
机制:特异性识别O²-苄基胞嘧啶(BC)配体。
正交性:尽管与SNAP-tag同源,但CLIP-tag对其底物具有高度特异性,两者交叉反应极低,适用于双重标记实验。
三、应用场景与优势
1、超越荧光蛋白的光物理性能
有机染料通常比荧光蛋白亮10倍以上,且具有更佳的光稳定性。利用HaloTag或SNAP-tag标记目标蛋白,可显著提升对低丰度蛋白或微弱结构的检测灵敏度。
同时,这些特性使其成为超分辨率显微镜(如STED、STORM)和单分子追踪技术的理想选择。
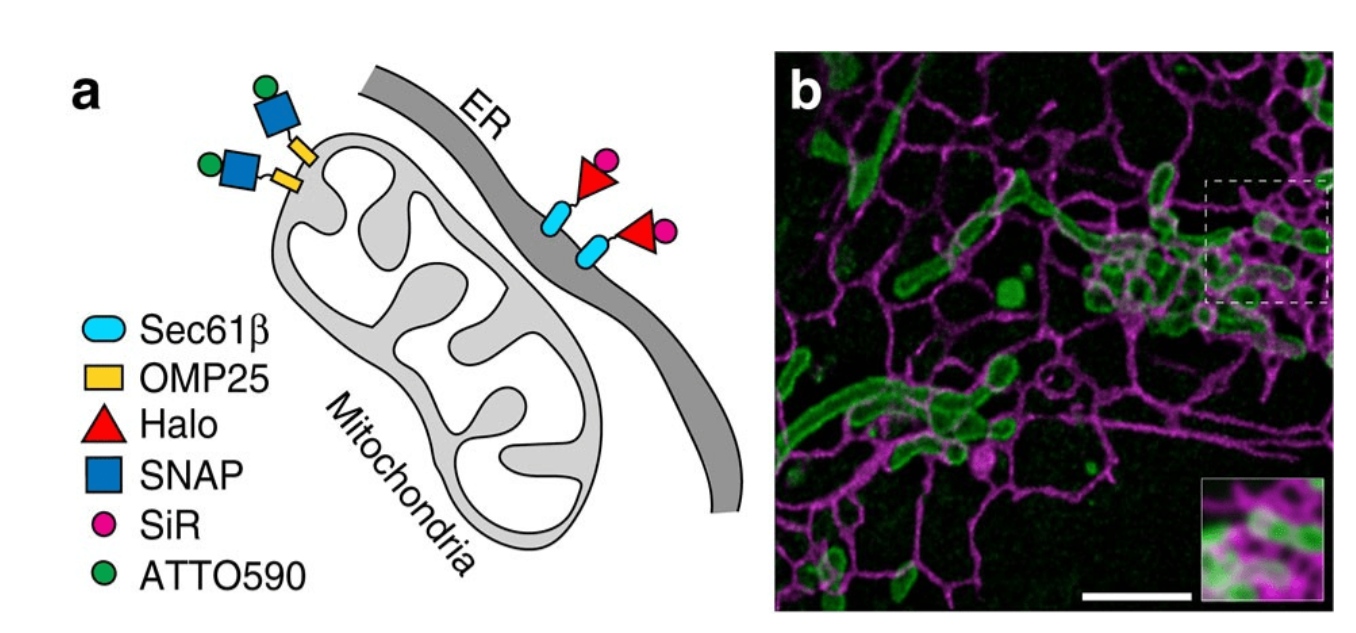
图2:对内质网和线粒体进行双色超分辨率成像,揭示了动态细胞器相互作用。
a)标记方案。
b) COS-7细胞内质网用Halo-Sec61β标记SiR-CA(品红色),外线粒体膜用SNAP-OMP25标记并带有Atto590-BG(绿色),并用受激发射耗竭(STED)纳米镜成像。
比例尺,2微米。插入图展示了与标准共聚焦显微镜的比较。图片改编自(Bottanelli 等,2016),采用CC-BY许可。
2、多色成像与正交标记
通过将不同的正交自标记标签(如SNAP-tag与CLIP-tag,或自标记标签与荧光蛋白)融合至不同目标蛋白,可实现高效的多色成像。
此外,在体外实验中,可对纯化的同一标签融合蛋白分别标记不同颜色的染料,随后重组复合物,灵活定制实验颜色方案。
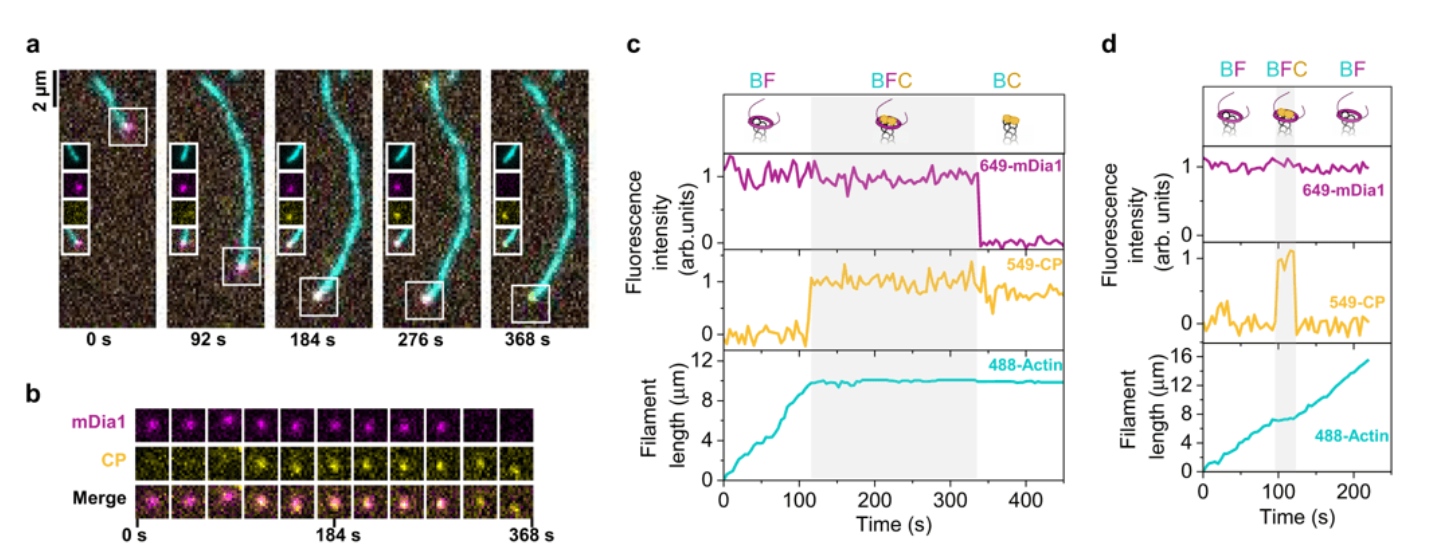
图3:体外单分子追踪肌动蛋白丝状体组装蛋白,揭示复杂事件。
a) 荧光标记肌动蛋白丝(488-肌动蛋白,青色)显微照片,尖端有甲胺(649-mDia1,品红)和盖蛋白(549-CP,黄色)。649-mDia1和549-CP都是SNAP标签融合体,经过纯化后分别用不同染料标记。
b) mDia1 和 CP 出现在丝尖(a)处。
c) 丝尖的强度痕迹从(a-b)处,显示649-mDia1或549-CP(上、中)的出现与消失,以及对肌动蛋白丝长度(下)的影响。
d)强度和丝长的痕迹,适用于CP短暂出现后离开的事件。图片重用自(Ulrichs 等,2023),采用CC-BY许可。
3、脉冲 - 追踪(Pulse-Chase)与动态更新
自标记技术极大简化了标签更新流程。研究者无需重新克隆即可尝试新型染料。更独特的是,利用配体的时间依赖性添加,可进行脉冲 - 追踪实验:
在不同时间点向同一细胞样本中添加不同颜色的配体,从而区分并追踪不同时段合成的蛋白亚群。例如,Cohen实验室利用HaloTag开发的“走马灯”策略,成功实现了细胞内记录的时间分辨标记。
4、超越成像:多功能修饰
自标记标签的应用远不止于荧光成像。通过偶联生物素、聚乙二醇(PEG)或磁珠等功能分子,该技术广泛应用于蛋白质纯化、表面固定及药物递送。
例如,张实验室近期利用SNAP-tag在合成病毒颗粒表面偶联抗体,实现了病毒载体的细胞类型特异性递送(Strebinger et al., 2023)。
四、局限性与选型策略
尽管灵活性极高,自标记标签也存在一定的局限性:
成本:商业化的有机染料配体价格通常高于细胞自主合成的荧光蛋白。
通透性:部分配体难以穿透细胞膜,限制了其在活细胞内部标记中的应用。
合成难度:若需自定义配体,可能涉及复杂的有机合成步骤(尽管商业选择日益丰富)。
选型建议:
特异性与尺寸权衡:
蛋白类标签(SNAP, CLIP, HaloTag)通常比短肽标签(如四半胱氨酸)具有更高的标记特异性。
若目标蛋白对空间位阻敏感,应优先考虑小尺寸标签:四半胱氨酸(~15 aa)< eDHFR(159 aa)≈ SNAP/CLIP(182 aa)< HaloTag(295 aa)。
相比之下,传统荧光蛋白通常为230–250 aa注:小尺寸并不绝对保证无功能干扰,仍需验证融合蛋白活性。
商业化与可获得性:
HaloTag与SNAP-tag拥有最丰富的商业配体库(供应商如Promega, NEB),且质粒资源易得。
CLIP-tag、TMP-tag及四半胱氨酸染料的商业选择相对较少,可能需要自行合成或寻找特定供应商。
反应动力学与应用场景:
不同标签与特定配体的反应速率存在差异(Wilhelm et al., 2021)。例如,HaloTag在某些染料标记中反应更快,而SNAP-tag在非荧光配体标记中表现更佳。
对于远红波段超分辨率成像,HaloTag配合特定罗丹明染料通常优于SNAP-tag(Erdmann et al., 2019)。
结论
自标记蛋白标签技术打破了传统荧光蛋白融合的僵化模式,将“基因编码”与“化学修饰”的优势完美结合。
它不仅解决了实验室中质粒冗余的痛点,更为动态生物学过程的解析提供了强大的工具箱。
在选择合适的标签时,研究者应综合考量实验目的、蛋白特性、成本预算及配体可用性,以充分发挥这一“化学魔法”的潜力。
参考文献
博塔内利,F.,克罗曼,E. B.,奥尔盖耶,E. S.,埃尔德曼,R. S.,伍德·巴格利,S.,西里纳基斯,G.,谢帕茨,A.,巴德利,D.,图姆雷,D. K.,罗斯曼,J. E.,和贝沃斯多夫,J.(2016)。细胞内靶标的双色活细胞纳米尺度成像。《自然通讯》,7(1),第1条。https://doi.org/10.1038/ncomms10778
埃尔德曼,R. S.,巴格利,S. W.,里琴斯,J. H.,维斯纳,R. F.,习,Z.,奥尔盖耶,E. S.,钟,S.,汤普森,A. D.,洛威,N.,巴特勒,R.,贝沃斯多夫,J.,罗斯曼,J. E.,约翰斯顿,D. S.,谢帕茨,A.,和图姆雷,D.(2019)。标记策略对超分辨率显微镜至关重要:HaloTag与SNAP标签的比较。《细胞化学生物学》,26(4),584-592.e6。https://doi.org/10.1016/j.chembiol.2019.01.003
加拉格尔,S. S.,萨布尔,J. E.,希茨,M. P.,和科尼什,V. W.(2009)。一种基于近距离诱导反应性的体内共价TMP标签。《美国化学会化学生物学》,4(7),547–556。https://doi.org/10.1021/cb900062k
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-03-24
编制人:大刘
审稿人:小藻
