微生物驱动代谢的底层能量运行方式
来源:武汉市灰藻生物科技有限公司 浏览量:82 发布时间:2026-03-29 17:20:13
能量与功
能量可以简单定义为,做功的能力。 所有物理和化学过程都是,能量应用或转移的结果。
活细胞主要进行三种功:
化学功 涉及从简单前体分子,合成复杂生物分子(即合成代谢);增加细胞的分子复杂性需要能量。
运输功 需要能量来摄取营养、排出废物并维持离子平衡。 输入能量是因为分子和离子通常需要逆电化学梯度跨细胞膜运输。
例如,即使细胞内浓度更高,分子仍会进入细胞。 同样,溶质可能逆浓度梯度被排出细胞。
第三种是 机械功,或许是三者中最熟悉的。 细胞运动以及细胞内结构的移动,都需要能量。
热力学定律
要理解能量如何以ATP形式捕获,以及ATP如何用于细胞做功,需要了解一些热力学基本原理。
热力学分析一个称为“系统”的物质集合(如一个细胞或一株植物)中的能量变化。 宇宙中所有其他物质称为“环境”。
热力学关注,系统起始状态和最终状态之间的能量差异,不关心过程速率。
例如,将一锅水加热至沸腾,热力学只关心水的起始和沸腾状态,而不关心加热速度或炉灶类型。
热力学第一定律 指出,能量不能被创造也不能被消灭。
宇宙中的总能量保持恒定,尽管可以重新分配,就像在化学反应中,发生的许多能量交换一样。
例如,放热反应释放热量,吸热反应吸收热量。
然而,仅凭第一定律无法解释,为什么一个反应放热而另一个吸热,也无法解释,为什么气体会从满钢瓶,流向空钢瓶,直到两瓶气压相等。
解释这些现象需要 热力学第二定律 和一个称为“熵”的物质状态属性。 熵可以被视为系统随机性或无序性的度量。 系统的无序性越大,其熵就越大。
第二定律指出,物理和化学过程总是朝着使宇宙(系统及其环境)的随机性或无序性增加到最大可能的方向进行。 气体总会膨胀到空钢瓶中。
需要定量说明特定过程中使用或产生的能量大小,有两种能量单位。 卡路里 是将一克水从14.5℃升高到15.5℃所需的热能。
能量也可以用 焦耳 表示,这是所能做的功的单位。 1卡路里热量相当于4.1840焦耳的功。 一千卡路里或1大卡的能量足以煮沸1.9毫升水。
1千焦耳的能量足以煮沸约0.44毫升水,或让一个体重70公斤的人爬35级台阶。
焦耳通常由化学家和物理学家使用。 由于生物学家最常用卡路里表示能量。
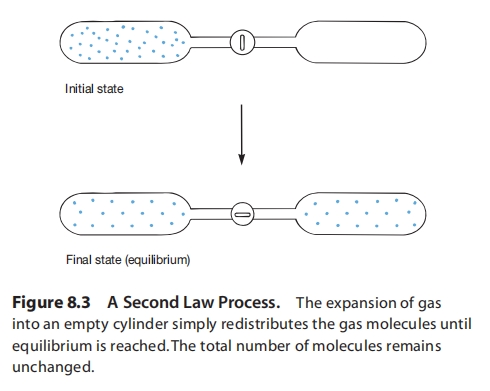
气体膨胀到空钢瓶中,只是重新分布气体分子直至达到平衡,分子总数保持不变。
自由能与反应
第一和第二定律可以结合成一个有用的方程,用于关联化学反应和其他过程中可能发生的能量变化。
ΔG = ΔH - T·ΔS
ΔG 是自由能变化,ΔH 是焓变化,T 是开尔文温度(摄氏度+273),ΔS 是反应中发生的熵变化。 焓变化是热含量变化。 细胞反应在恒压恒容条件下发生。
因此,焓变化大致等于反应中总能量的变化。 自由能变化是系统(或细胞)在恒温恒压下可用于做有用功的能量。
因此,熵变化(ΔS)衡量了系统,无法用于做功的那部分总能量,变化的比例。
自由能和熵的变化不取决于系统从起点到达终点的路径。 如果反应过程中系统的自由能减少,或者说如果ΔG为负,反应将自发进行。
从方程可知,熵变化为正且较大的反应通常倾向于具有负的ΔG值,因此会自发进行。 熵减少则倾向于使ΔG更正,反应变得不利。
可以将熵变化(ΔS)与自由能变化(ΔG)的关系想得更具体些。
想想希腊神话中的科林斯国王西西弗斯。 因犯下罪行,他被罚永无止境地将巨石滚上陡峭的山顶。
这代表着非常大的负熵变化——停在陡坡顶部的巨石既不随机也无序——而这项活动具有非常大的正ΔG。
也就是说,西西弗斯必须向系统输入大量能量。 不幸的是,巨石一到山顶,就会自发滚回山下。 这代表了正的熵变化和负的ΔG。
西西弗斯不需要再输入能量,他可能只是站在山顶看着反应进行。
自由能变化与化学反应的方向也有明确、具体的关系。 考虑这个简单反应:
A + B ⇌ C + D
如果将A和B分子混合,它们会结合生成产物C和D。 最终C和D会变得足够浓,它们结合生成A和B的速率与A和B生成C和D的速率相同。
此时反应达到 平衡:两个方向的速率相等,反应物和产物的浓度不再发生净变化。 这种情况由 平衡常数(Keq)描述,它关联了平衡时产物和底物的浓度:
Keq = [C][D] / [A][B]
如果平衡常数大于1,平衡时产物浓度高于反应物浓度,即反应倾向于按反应式方向进行完全。
反应的平衡常数与其自由能变化直接相关。 当在严格定义的标准条件(浓度、压力、pH和温度)下测定过程的自由能变化时,称为 标准自由能变化(ΔG°)。
如果pH设定为7.0(接近活细胞pH),标准自由能变化用符号ΔG°′表示。 标准自由能变化可以看作是标准条件下系统可用于做有用功的最大能量。
使用ΔG°′值可以在不考虑因环境条件差异引起的ΔG变化的情况下比较反应。 ΔG°′与Keq的关系由下式给出:
ΔG°′ = -2.303RT·log Keq
R是气体常数(1.9872 cal/mol·度 或 8.3145 J/mol·度),T是绝对温度。 观察此方程可知,当ΔG°′为负时,平衡常数大于1,反应按反应式方向进行完全。
这称为 放能反应。 在 吸能反应 中,ΔG°′为正,平衡常数小于1。 也就是说,反应不利,在标准条件下平衡时产物生成量很少。
记住,ΔG°′值只显示反应在平衡时的位置,不显示反应达到平衡的速度。
ΔG°′ 与平衡: ΔG°′ 与反应平衡的关系。注意放能反应和吸能反应之间的差异。
ATP在代谢中的作用
如前所述,微生物世界存在相当大的代谢多样性。
然而,有几种生化原理是所有类型代谢共有的:
(1)利用ATP在放能反应中捕获能量,以便用于驱动吸能反应;
(2)将代谢反应组织成途径和循环;
(3)通过酶催化代谢反应;
(4)氧化还原反应在能量保存中的重要性。
本节将探讨,ATP在代谢中的作用。
能量从细胞的能量来源以放能反应(即ΔG为负的反应)释放。 这些能量大部分被以实用形式捕获,而不是浪费掉,从而可以转移到进行做功的细胞系统中。
这些系统进行吸能反应(即合成代谢),细胞利用捕获的能量驱动这些反应进行完全。 在生物体中,这种实用形式的能量是 腺苷5′-三磷酸(ATP)。
从某种意义上说,细胞进行某些过程是为了“赚取”ATP,并利用其他过程来“花费”ATP。
因此,ATP常被称为细胞的能量货币。 在细胞的经济体系中,ATP充当了放能反应和吸能反应之间的连接物。
是什么使得ATP适合扮演能量货币这一角色? ATP是一种高能分子。 也就是说,它分解或水解为腺苷二磷酸(ADP)和正磷酸盐(Pi)几乎完全,其ΔG°′为-7.3 kcal/mol:
ATP + H2O → ADP + Pi
将ATP称为高能分子并不意味着其特定键中储存了大量能量。 它只是表示末端磷酸基团的去除进行完全,且具有较大的负标准自由能变化;也就是说,该反应是强放能的。
因为ATP容易将其磷酸基团转移到水,所以说它具有高的 磷酸基团转移势能,定义为水解去除磷酸基团的ΔG°′的负值。 具有更高基团转移势能的分子会将磷酸基团捐赠给势能较低的分子。
虽然ATP水解的自由能变化相当大,但还有许多反应释放更多的自由能。 这些能量在分解代谢和其他能量保存过程中用于从ADP和Pi重新合成ATP。
同样,分解代谢可以产生比ATP具有更高磷酸基团转移势能的分子。 细胞利用这些分子通过一种称为 底物水平磷酸化 的机制从ADP再生ATP。
因此,ATP、ADP和Pi形成了一个能量循环。 供能反应 通过利用从能源释放的能量合成ATP来保存能量。
当ATP水解时,释放的能量驱动吸能过程,如合成代谢、运输和机械做功。 合成ATP的机制将在第9章详细描述。
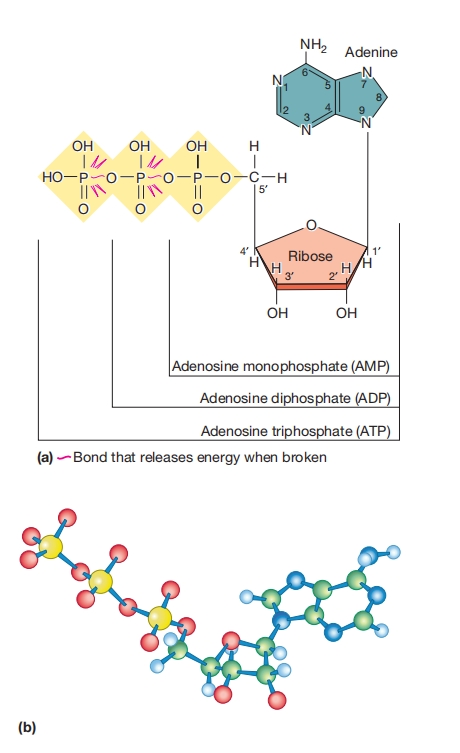
腺苷三磷酸和腺苷二磷酸。
(a)ATP、ADP和AMP的结构。两条红色键更容易断裂或具有高磷酸基团转移势能(见正文)。
嘧啶环原子已编号,核糖中的碳原子也已编号。
(b)ATP模型。碳为绿色;氢为浅蓝色;氮为深蓝色;氧为红色;磷为黄色。
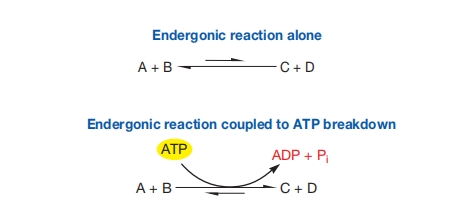
ATP用于使吸能反应更易进行。它由放能反应形成,然后用于驱动吸能反应。
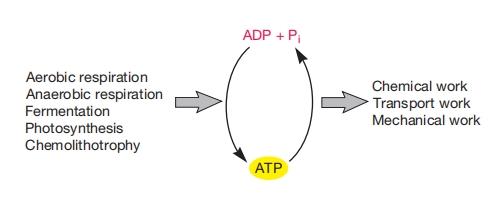
ATP由有氧呼吸、无氧呼吸、发酵、化能无机营养和光合作用过程中释放的能量形成。其分解为ADP和磷酸(Pi)使得化学功、运输功和机械功得以进行。
氧化还原反应、电子载体与电子传递系统
自由能变化与所有化学反应的平衡相关,包括氧化还原反应的平衡。 从能源释放能量通常涉及氧化还原反应。 氧化还原反应 是电子从电子供体转移到电子受体的反应。
按惯例,此类反应写为供体在右,受体在左,并注明转移的电子数n。
受体和供体对称为 氧化还原对。 当受体接受电子时,它就变成了该对的供体。 反应的平衡常数称为 标准还原电位(E0),是衡量供体失去电子倾向的指标。 还原电位的参考标准是氢系统,其E0′(pH 7.0下的还原电位)为-0.42伏或-420毫伏。
2H+ + 2e- ⇌ H2
在此反应中,每个氢原子提供一个质子(H+)和一个电子(e-)。 如前所述,标准还原电位以伏特或毫伏为单位。 伏特是电势或电动势的单位。 因此,像氢系统这样的氧化还原对是潜在的能源。
还原电位有具体含义。 还原电位较负的氧化还原对会将电子捐赠给还原电位更正(对电子亲和力更大)的氧化还原对。
因此,电子倾向于从表8.1中列表顶部的供体流向底部的受体,因为后者具有更正的电位。 这可以用 电子塔 直观地表示,最负的还原电位位于顶部。
电子从供体流向受体,顺着电位梯度下降,或从塔上落到更正的电位处。
以电子载体 烟酰胺腺嘌呤二核苷酸(NAD+)为例。 NAD+/NADH对的E0′非常负,因此可以将电子提供给许多受体,包括O2:
NAD+ + 2H+ + 2e- ⇌ NADH + H+ E0′ = -0.32 V 1/2 O2 + 2H+ + 2e- ⇌ H2O E0′ = +0.82 V
因为NAD+/NADH的还原电位比1/2 O2/H2O的更负,电子将从NADH(供体)流向O2(受体):
NADH + H+ + 1/2 O2 → H2O + NAD+
由于NAD+/NADH对的E0′相对较负,它比还原电位较不負(或更正)的氧化还原对储存更多的势能。 因此,当电子从供体移动到具有更正还原电位的受体时,会释放自由能。
反应的ΔG°′与两个氧化还原对还原电位差(ΔE0′)的大小直接相关。 ΔE0′越大,可获得的自由能就越大,如下式所示:
ΔG°′ = -nF·ΔE0′
其中n是转移的电子数,F是法拉第常数(23,062 cal/mol·V 或 96,494 J/mol·V)。 对于双电子转移,ΔE0′每变化0.1伏特,ΔG°′相应变化4.6 kcal。
这类似于其他化学反应中ΔG°′与Keq的关系——平衡常数越大,ΔG°′越大。 NAD+/NADH与1/2 O2/H2O之间的还原电位差为1.14伏特,这是一个很大的ΔE0′值。
当电子从NADH移动到O2时,大量自由能被释放用于合成ATP。
我们重点关注NADH还原O2的过程,因为NADH在许多生物(尤其是化能有机营养生物)的代谢中起核心作用。 许多化能有机营养生物利用葡萄糖作为能源。
葡萄糖被分解代谢时,被氧化。 葡萄糖释放的许多电子被NAD+接受,NAD+被还原为NADH。 NADH随后将电子传递给O2。 然而,它并非直接传递。
相反,电子通过一系列电子载体传递给O2。 这些电子载体组织成一个称为 电子传递系统(ETS)或电子传递链。
这些载体的组织方式使得第一个电子载体具有最负的E0′,每个后续载体的E0′略微减小(更不負)。 这样,储存在启动电子流的氧化还原对中的势能被释放并用于形成ATP。
化能有机营养生物的ETS位于原核生物的质膜和真核生物的内线粒体膜中。 电子传递系统在化能无机营养生物和光养生物的新陈代谢中也起关键作用,分别用于保存来自无机能源和光的能量。
ETS位于化能无机营养生物(均为原核生物)的质膜或内膜系统中。 它们位于原核光养生物的质膜和内膜系统,以及真核光养生物叶绿体的类囊体膜中。
构成ETS的载体在化学性质及其携带电子的方式上有所不同。 NAD+及其化学近亲 烟酰胺腺嘌呤二核苷酸磷酸(NADP+)含有一个烟酰胺环。
这个环从供体(例如葡萄糖分解代谢过程中形成的中间体)接受两个电子和一个质子,并释放第二个质子。
黄素腺嘌呤二核苷酸(FAD)和 黄素单核苷酸(FMN)在复杂的环系统上携带两个电子和两个质子。 携带FAD和FMN的蛋白质通常称为 黄素蛋白。
辅酶Q(CoQ)或 泛醌 是一种醌类,在许多电子传递链中运输两个电子和两个质子。 细胞色素 和其他几种载体利用铁原子通过可逆的氧化还原反应一次运输一个电子:
Fe3+(三价铁) + e- ⇌ Fe2+(二价铁)
在细胞色素中,这些铁原子是血红素基团的一部分,或其他类似的铁-卟啉环。 几种不同的细胞色素(每种都由蛋白质和铁-卟啉环组成)是电子传递链的重要组成部分。
一些含铁电子载体蛋白缺乏血红素基团,称为 非血红素铁蛋白。 铁氧还蛋白 是一种非血红素铁蛋白,活跃于光合电子传递和其他几个电子传递过程中。
尽管其铁原子不与血红素基团结合,它们仍然经历可逆的氧化还原反应。 与细胞色素一样,它们一次只携带一个电子。
这种携带电子和质子数量的差异在电子传递链的运行中非常重要,将在第9章进一步讨论。
生物学重要氧化还原对
| 氧化还原对 | E0′ (伏特) |
|---|---|
| 2H+ + 2e- → H2 | -0.42 |
| 铁氧还蛋白 (Fe3+) + e- → 铁氧还蛋白 (Fe2+) | -0.42 |
| NAD(P)+ + H+ + 2e- → NAD(P)H | -0.32 |
| S + 2H+ + 2e- → H2S | -0.274 |
| 乙醛 + 2H+ + 2e- → 乙醇 | -0.197 |
| 丙酮酸 + 2H+ + 2e- → 乳酸2- | -0.185 |
| FAD + 2H+ + 2e- → FADH2 | -0.18 |
| 草酰乙酸2- + 2H+ + 2e- → 苹果酸2- | -0.166 |
| 延胡索酸2- + 2H+ + 2e- → 琥珀酸2- | 0.031 |
| 细胞色素 b (Fe3+) + e- → 细胞色素 b (Fe2+) | 0.075 |
| 泛醌 + 2H+ + 2e- → 泛醌 H2 | 0.10 |
| 细胞色素 c (Fe3+) + e- → 细胞色素 c (Fe2+) | 0.254 |
| 细胞色素 a (Fe3+) + e- → 细胞色素 a (Fe2+) | 0.29 |
| 细胞色素 a3 (Fe3+) + e- → 细胞色素 a3 (Fe2+) | 0.35 |
| NO3- + 2H+ + 2e- → NO2- + H2O | 0.421 |
| NO2- + 8H+ + 6e- → NH4+ + 2H2O | 0.44 |
| Fe3+ + e- → Fe2+ | 0.771 |
| O2 + 4H+ + 4e- → 2H2O | 0.815 |
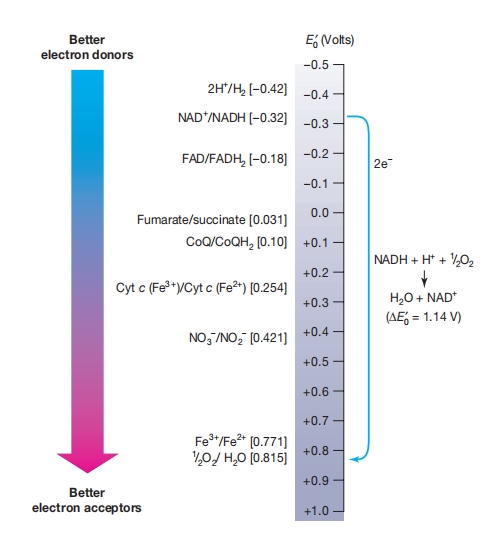
电子移动与还原电位。 此图中的垂直电子塔顶部为最负的还原电位。电子会自发地从塔上较高位置(更负电位)的供体流向塔上较低位置(更正电位)的受体。
也就是说,供体在塔上的位置总是高于受体。例如,NADH会将电子捐赠给氧气并在此过程中形成水。左侧显示了一些典型的供体和受体,其氧化还原电位标在括号中。
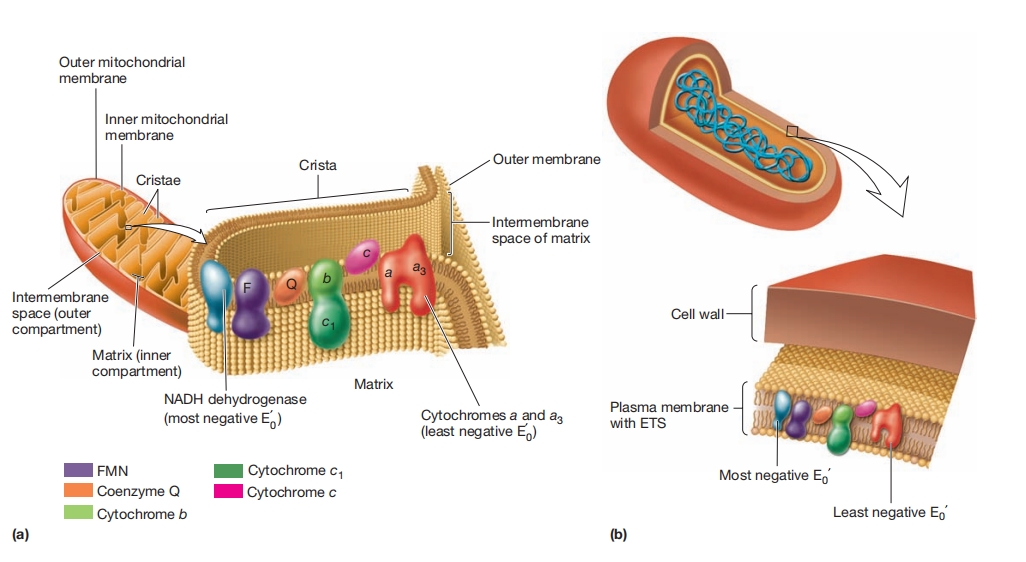
电子传递系统。 电子传递系统(ETS)位于膜中。在呼吸过程中(有氧呼吸、无氧呼吸和化能无机营养),电子从具有最负还原电位的电子载体流向具有最正还原电位的电子载体。
该图显示了电子传递链,其中氧气(有氧呼吸)或其他物质(无氧呼吸)作为最终电子受体。(a)线粒体ETS。(b)典型的细菌ETS。
参考文献
《Microbiology (Seventh Edition)》 | 微生物学(第七版),第8节
相关产品
| 货号 | 名称 | 价格 | 规格 |
|---|---|---|---|
| HZB875586 | 碎肉碳水化合物肉汤培养基 | 350 | 250g/瓶 |
| HZB875648 | 庖肉牛肉粒 | 230 | 100g/瓶 |
| HZB875647 | 氯化血红素 | 60 | 5ml/支(0.1mg/ml)、5支/盒 |
| HZB875646 | 维生素K1 | 50 | 5ml/支(1mg/ml)、5支/盒 |
| HZB875650 | L-半胱氨酸盐酸溶液 | 60 | 1ml/支(0.05g/ml),5支/盒 |
敬请关注灰藻生物,共筑健康未来!— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-03-31
编制人:小藻
审稿人:小藻
