非乳酸菌及其他新型益生菌在健康及生物技术的应用
来源:武汉市灰藻生物科技有限公司 浏览量:150 发布时间:2026-03-25 20:46:09
一、摘要
营养学家与健康专家,对具有促进健康(pro-health)特性的微生物,及其在预防感染性和非感染性疾病方面作用的兴趣日益高涨,进一步推动了对多样化益生菌微生物的研究。
随着对微生物健康益处认知的不断扩展,科研人员正积极,从各类微生物生态位(microbiological niches)中,发掘可用于健康及生物技术(益生菌)应用的新型微生物。
对于新近发现的未来型非乳酸菌(non-lactic acid bacteria, non-LAB)益生菌:
如 Akkermansia muciniphila(嗜黏蛋白阿克曼菌)、Bacillus spp.(芽孢杆菌属)、Faecalibacterium prausnitzii(普拉梭菌)、Roseburia spp.(罗氏菌属)以及酵母(如 Saccharomyces boulardii,布拉氏酵母菌),其最优先关注的问题应是最佳剂量(optimal dose)。
二、 引言
微生物在营养学、生物医学及兽医学中具有极其重要的地位。由于具备“一般认为安全”(Generally Recognized As Safe, GRAS)资质,乳酸菌(Lactic Acid Bacteria, LAB)被广泛用作益生菌。
目前商品化益生菌产品中主要包含七个属的微生物:Lactobacillus(乳杆菌属)、Bacillus(芽孢杆菌属)、Bifidobacterium(双歧杆菌属)、Enterococcus(肠球菌属)、Escherichia(埃希氏菌属)、Streptococcus(链球菌属)以及酵母(如 Saccharomyces 和其他属)。
近年来,从成人胃肠道(GI tract)、人乳及婴儿体内等生境中已鉴定出多种具有有益特性的非乳酸菌(non-LAB),这些菌株展现出多重促健康功能,因而被视为极具潜力的未来型益生菌,适用于营养、健康及生物技术领域。
除传统发酵食品(如蔬菜、泡菜、乳制品和发酵肉制品)中的益生菌外,来自其他来源的新型微生物也引起了微生物生态学家以及食品、饲料和制药工业界的广泛关注。这些微生物或因过去未被发现,或因其特性尚未被充分阐明。
三、新型益生菌的营养、健康及疾病缓解特性
尽管传统益生菌,在营养与疾病缓解方面的功效,已被广泛研究,但诸如 Akkermansia muciniphila、Bacteroides thetaiotaomicron(多形拟杆菌)、Christensenella minuta(微小克里斯滕森菌)、Faecalibacterium prausnitzii、Hafnia alvei(蜂房哈夫尼菌)和 Parabacteroides goldsteinii(戈氏副拟杆菌)等新型益生菌因其治疗与预防潜力,正接受科学界深入分析。初步研究表明,这些微生物在抵御肠道疾病、炎症及癌症方面具有保护作用。
例如,Hafnia alvei HA4597® 菌株可产生一种名为 ClpB 的饱腹感肽(satietyogenic peptide),该肽可模拟 α-黑素细胞刺激激素(α-MSH)的作用,已在实验动物中证实可调控食欲、肥胖及体重增长,虽在人体中前景广阔,但仍需进一步研究验证。
以下对若干重要非乳酸菌益生菌进行综述。
四、产乙酸菌
肠道微生物发酵摄入的植物细胞壁多糖所产生的短链脂肪酸(Short-Chain Fatty Acids, SCFAs)具有多重治疗益处,包括免疫调节、能量代谢及脑功能调控。
参与SCFA生成的微生物因此被视为具有多重健康益处的益生菌。
例如,肠道细菌 Christensenella minuta(菌株 DSM22607)可高效产生乙酸(acetate),并少量生成丁酸(butyrate),表现出显著的抗炎活性:
通过抑制 NF-κB 信号通路降低 IL-8 细胞因子水平,减轻结肠炎症,促进黏膜修复,并保护肠道上皮完整性。基于上述益生特性,C. minuta 有望成为治疗炎症性肠病(IBD)的新型微生物疗法。
五、 产丁酸菌
游离态SCFAs是肠道微生物的关键代谢物,不仅为结肠细胞提供能量来源,还能维持肠道屏障健康、预防癌症,并参与多种生理与认知活动。
SCFAs还可通过孤儿G蛋白偶联受体(如 GPR41 和 GPR43)刺激肠道肽(如胰高血糖素样肽 GLP 或肽YY PYY)分泌,从而调控葡萄糖代谢与摄食行为。
丁酸作为植物多糖微生物发酵的主要产物,在胃肠道中具有多种关键功能。在IBD等疾病中,丁酸及其产生菌常显著减少,因此补充产丁酸菌具有治疗价值。
产丁酸菌被视为下一代益生菌,对IBD患者尤为重要。此外,2型糖尿病(T2DM)患者肠道中产丁酸菌丰度下降,提示其在T2DM病理生理中的潜在作用。
产丁酸菌还参与认知功能调节。肥胖人群易患神经退行性疾病及认知障碍,其肠道菌群-脑轴(gut microbiota–brain axis)存在明显失调。
一项研究发现,肥胖人群中 Clostridium butyricum(丁酸梭菌)减少,而变形菌门(Proteobacteria)丰度增加。
在高脂低纤“西方饮食”诱导的肥胖小鼠模型中,将健康供体小鼠粪便中的 C. butyricum 通过粪菌移植(FMT)给予肥胖小鼠,可改善结肠完整性并提升认知能力。
直接喂食纯 C. butyricum 菌株可防止菌群失调、增强肠道屏障、改善认知功能,并缓解海马神经突生长及突触超微结构缺陷,其机制与海马突触和树突相关转录组调控有关。
因此,C. butyricum 通过肠-菌群-脑轴对肥胖相关认知障碍具有神经保护作用。
5.1 嗜黏蛋白阿克曼菌
Akkermansia muciniphila 是一种定植于人类肠道黏液层的黏蛋白降解共生菌。该菌为革兰氏阴性、卵圆形、严格厌氧、不产芽孢的细菌,最早于2004年由荷兰瓦赫宁根大学(Wageningen University)在筛选能降解肠道黏蛋白的微生物时被发现。
它是目前已知唯一存在于人类肠道中的疣微菌门(Verrucomicrobia)成员。非培养研究亦在煮沸牛奶中检测到该菌。
基于对39株源自人和小鼠粪便的 A. muciniphila 全基因组测序(WGS)分析,揭示了其遗传多样性与独特代谢特征。
定量研究显示,该菌与人体体重指数(BMI)及降糖药物使用密切相关。在肠道菌群演化过程中,A. muciniphila 可能从邻近共生菌获得了抗生素抗性基因。
尽管最初被归类为严格厌氧菌(对氧敏感),但后续研究表明,其与 Bacteroides fragilis(脆弱拟杆菌)和 Bifidobacterium adolescentis(青春双歧杆菌)类似,
可耐受低浓度氧气,这种耐受性为其生长提供了优势。
鉴于其在代谢调控(抗肥胖、抗糖尿病效应)及免疫调节中的潜力,A. muciniphila 在癌症治疗等领域备受关注。
然而,目前多数益处证据来自体外实验或动物模型,其在人体中的安全性与有效性仍需严格评估。
5.2 芽孢杆菌属
与其他益生菌不同,Bacillus spp. 因其天然产芽孢能力,可分泌多种蛋白质、酶、抗菌物质、维生素及类胡萝卜素,数百年来被用于食品生产与保藏。
此外,芽孢杆菌耐受食品加工与胃肠道环境,能与宿主内环境互作,合成抗菌肽(AMPs)及胞外效应分子,使其成为多功能菌种。
然而,由于对其“益生菌 vs. 致病菌”身份的争议,芽孢杆菌尚未获得应有的认可。消费者需清晰了解拟用作益生菌的芽孢杆菌株的表型与基因型特征。
芽孢杆菌可生产食品级淀粉酶、葡萄糖淀粉酶、蛋白酶、果胶酶和纤维素酶。例如,Bacillus licheniformis ATCC 14580 产生的植酸酶广泛应用于生物技术及人畜营养。
Bacillus megaterium(巨大芽孢杆菌)作为GRAS微生物,是厌氧合成维生素B12(氰钴胺)的理想模型,亦可生产核黄素、肌醇、钴胺素及类胡萝卜素。
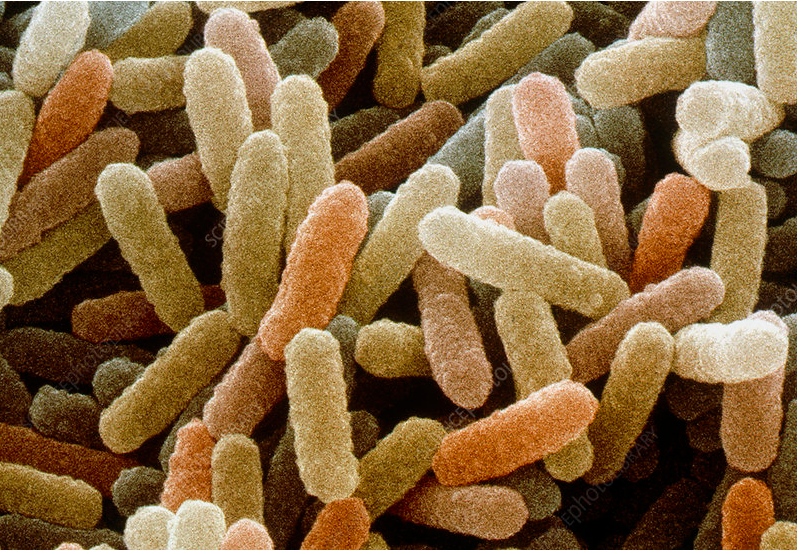
图1.Bacillus sp. 细菌的彩色扫描电子显微镜图像
5.3 丁酸球菌
Butyricoccus pullicaecorum 是一种安全的厌氧菌,已被证明对人类具有潜在益生作用。其模式菌株 25-3T 首次被证实可产丁酸,且在动物与人体志愿者中安全。
该菌在4°C下商业制剂中封装后可稳定存活8个月,并保持促健康特性,被视为下一代益生菌候选者。
该菌最初从4周龄肉鸡盲肠内容物中分离,属于梭菌簇IV(clostridial cluster IV),有望用于改善胃肠道健康、缓解IBD及结直肠癌。
口服 B. pullicaecorum 可耐受胃部酸性环境(pH 2.0–3.0),进入小肠碱性环境后恢复增殖。其丁酸产物对膀胱尿路上皮癌细胞系(HT1376)具有抗癌作用,
可通过调控细胞周期、抑制增殖,并上调膀胱癌相关蛋白(BLCAP)基因表达,诱导细胞凋亡。
此外,Clostridium butyricum 可显著抑制高脂饮食诱导的 Apcmin/+ 小鼠肠道肿瘤发展,抑制Wnt/β-catenin信号通路,调节有益菌群,提升SCFAs水平,降低次级胆汁酸。
产丁酸菌还可合成维生素、抗癌物质、抗炎分子,修复菌群生态,抑制病原菌。肠道丁酸通过调控组蛋白去乙酰化酶(HDAC)维持屏障功能并预防癌症。
深入理解丁酸生成及其代谢调控,有望为代谢性疾病治疗提供新思路。
5.4 纽约杜博氏菌
Dubosiella newyorkensis 最初于2017年从小鼠肠道中分离,被认为是一种具有多重健康益处的潜在益生菌,包括抗肥胖、降血压、抗氧化、护肝及抗衰老作用,并可预防年龄相关疾病。
小鼠模型研究表明,其抗衰老效应源于对肠道 Bifidobacterium(双歧杆菌)、Lactobacilli(乳杆菌)及 Ileibacterium(回肠杆菌)的正向调节。
其抗氧化与抗衰老效果可媲美甚至优于白藜芦醇(resveratrol)。
5.5 大肠杆菌Nissle 1917
Escherichia coli Nissle 1917(EcN)是由Alfred Nissle于1917年分离的非致病性革兰氏阴性菌株,是公认的益生菌。
其为德国Mutaflor®(Ardeypharm GmbH)及意大利EcM(Cadigroup)等微生物药物的活性成分,用于治疗胃肠道疾病。
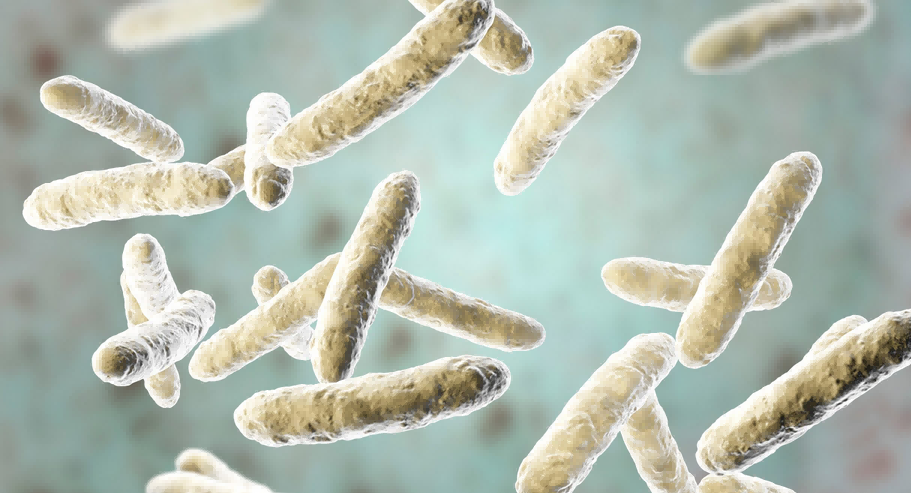
图2.大肠杆菌 Nissle 1917(Escherichia coli Nissle 1917)的显微图像
EcN及其基因工程改造株被用作“微型机器人工厂”,用于靶向肿瘤治疗。例如,改造后的EcN可表达细胞毒性化合物,或递送p53与Tum-5以治疗实体瘤。
Ho等人将EcN改造为表达金黄色葡萄球菌组蛋白样蛋白,使其能结合结直肠癌(CRC)细胞表面的硫酸乙酰肝素蛋白聚糖(HSPG);同时表达芥子酶(myrosinase),将膳食硫代葡萄糖苷转化为抗癌物质萝卜硫素(sulforaphane),在体外对人和小鼠结肠腺癌细胞系抑制率达95%以上。
然而,EcN基因组中含有 pks 毒力岛,可合成大肠杆菌素(colibactin)——一种强效DNA烷基化剂,可能诱发真核细胞致癌突变。此风险需引起公共卫生部门与益生菌制造商高度重视。
5.6 普拉梭菌
F. prausnitzii 是一种重要的共生菌,在Caco-2细胞及TNBS结肠炎小鼠模型中均表现出抗炎活性。其可减轻TNBS诱导的结肠炎,改善菌群失调,有望成为克罗恩病(CD)的新疗法。
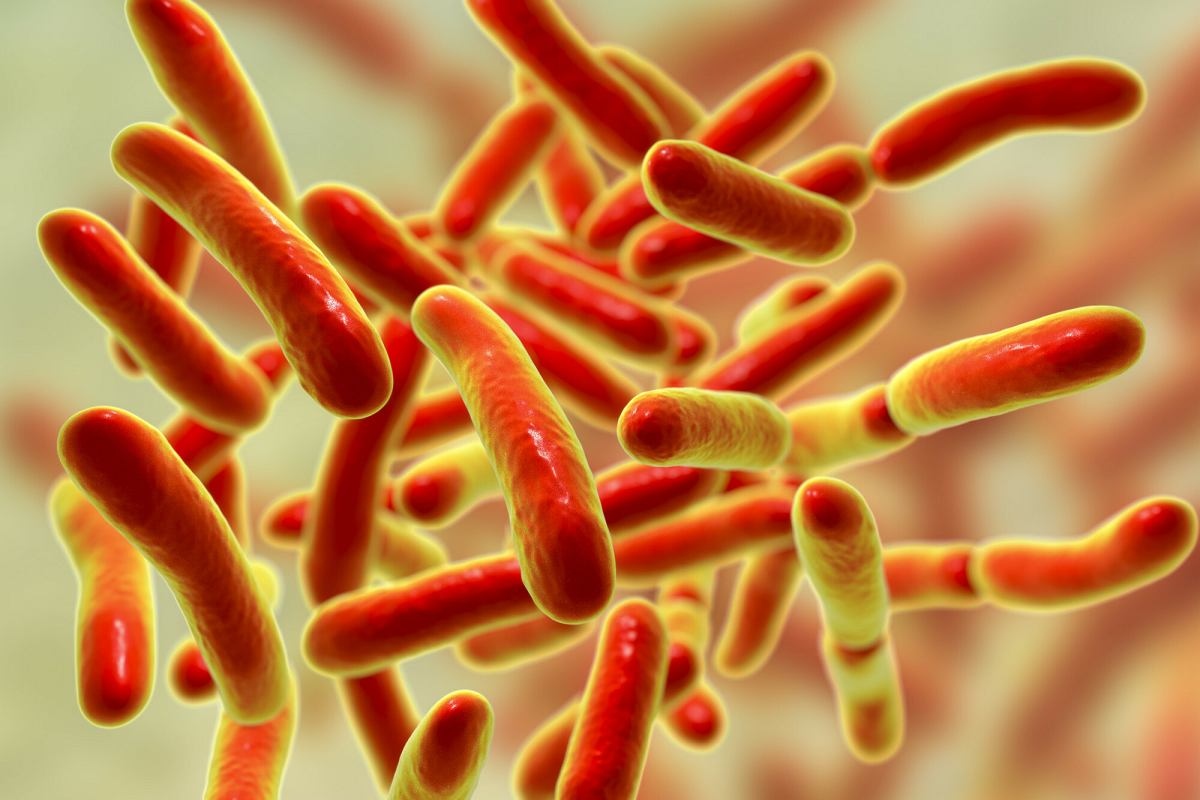
图3.普拉梭菌(Faecalibacterium prausnitzii)彩色扫描电子显微图像
健康人与IBD患者肠道菌群(尤其是厚壁菌门 Firmicutes 中的 F. prausnitzii)存在显著差异。该菌数量下降会使肠黏膜更易发生炎症,提示其对肠道稳态至关重要。
体外实验显示,F. prausnitzii 与丁酸产生菌组合可显著提升黏液相关菌群的丁酸浓度(5–11 mol%)及定植能力。此外,牛乳中亦检出 F. prausnitzii 菌株,提示乳源菌株或可作为粪菌移植的替代方案。
5.7 蜂房哈夫尼菌
H. alvei 属肠杆菌科(Enterobacteriaceae),1954年首次从生乳中分离,后见于传统奶酪。该菌为革兰氏阴性兼性厌氧杆菌,是人体肠道正常菌群成员之一。尽管部分菌株具机会致病性,但 HA4597™ 菌株在3–5%人群中自然存在(MEHAIT队列研究)。
该菌可产生 ClpB 蛋白,模拟α-MSH结构,与饥饿素(ghrelin)和瘦素(leptin)产生分子模拟,从而调控饱腹感。在ob/ob及高脂饮食肥胖小鼠中,H. alvei HA4597® 显著减少摄食量、体重及脂肪积累。
一项双盲随机对照试验(n=236)显示,每日服用1000亿CFU的HA4597® 12周后,受试者饱腹感增强、臀围减小,空腹血糖显著低于安慰剂组。
在三种肥胖小鼠模型中,HA4597®(1.4×10¹⁰ CFU/天,38天)的减重效果与标准饮食相当,并显著降低血糖、总胆固醇及丙氨酸氨基转移酶(ALT)。
5.8 罗氏菌属
Roseburia 为革兰氏阳性专性厌氧菌,形态直或微弯,具亚端鞭毛。包含5个种:R. ceciocola、R. faecis、R. hominis、R. intestinalis 和 R. inulivorans。该属定植于肠道,主要产丁酸,影响肠道蠕动、免疫及炎症反应。
5.9 鼠伤寒沙门氏菌
经减毒改造的非致病性 S. typhimurium 可表达 Vibrio vulnificus 的异源鞭毛蛋白B(FlaB),在小鼠肿瘤模型中激活TLR-5介导的先天抗肿瘤免疫,延长生存期且无毒性。
5.10 凝结魏茨曼菌
Weizmannia coagulans(原称 Bacillus coagulans)是从发酵乳品及谷物中分离的新型益生菌,兼具芽孢杆菌与乳杆菌特性。基因组分析显示其含细菌素(bacteriocin)合成基因簇及黏附相关基因,所产细菌素耐热耐酸。
EFSA评估认为,其菌株DSM 32789产生的乳酸在反刍动物和猪饲料中安全剂量为50,000 mg/kg,其他物种则更低。
饲喂 W. coagulans SANK70258 可上调肉鸡肠道免疫基因(IL-17A、IL-17F、IL-10、cathelicidin-2、pIgR),减少肠道损伤,促进增重,并富集 Alistipes 与 Enterococcus。
六、展望与挑战
肠道菌群作为“人体第二器官”及复杂生态系统,其健康价值已激发对非乳酸菌作为下一代益生菌的浓厚兴趣。这些新型益生菌有望在未来成为益生疗法与健康管理的核心组成部分。
多种微生物已被证实可调节肠道菌群。鉴于众多疾病受肠道微生态调控,通过优化菌群以改善宿主健康成为重要策略。
如 Butyricoccus pullicaecorum 等产丁酸菌已被视为下一代益生菌。
除乳制品发酵菌外,源自胃肠道及泌尿生殖道的微生物正成为新型益生菌来源。开发新型益生菌的关键步骤包括:设计合理保质期的制剂、通过动物模型及健康志愿者研究确证其安全性。
目前多数研究基于小鼠、大鼠、鸡和猪等动物模型。尽管新型益生菌可能耐热、耐胃酸并具抗菌活性,但在推荐用于营养或商业化前,必须确保其安全性。
七、结论
近几十年来,益生菌及有益微生物研究蓬勃发展。鉴于其多重促健康效益及疾病治疗新前景,非乳酸菌已引起微生物学家广泛关注。现有证据表明,Akkermansia muciniphila、Bacillus subtilis(枯草芽孢杆菌)、Bacillus licheniformis(地衣芽孢杆菌)、Clostridium butyricum、Escherichia coli Nissle 1917、Faecalibacterium prausnitzii 及 Roseburia hominis(人罗氏菌)等菌株可改善肠道微生态、促进营养利用(表1)。这些益生菌亟需在人类与动物中开展系统性评估。
表1.益生菌菌株的特性、研究方法及科学推论
| 益生菌(Probiotics) | 特性(Properties) | 研究方法(Methods of study) | 推论(参考文献)(Inferences (References)) |
|---|---|---|---|
| Akkermansia muciniphila | 肝脏保护作用(Hepatoprotective) | 小鼠肝损伤模型(In vivo/mouse model of liver injury) | 预防对乙酰氨基酚诱导的肝损伤,提高超氧化物歧化酶(SOD)水平,恢复肠道微生物群,并增加肠道微生物短链脂肪酸(SCFAs)(Xia等,2022) |
| 小鼠模型(In vivo/mouse model) | Akkermansia muciniphila介导的非酒精性脂肪肝病(MAFLD)和肝损伤的预防作用,在高胆固醇饮食喂养的肥胖小鼠模型中表现显著(Rao等,2021) | ||
| Bacillus spp. strains CHC 3810, CHCC 15541, B. licheniformis CHCC 3809, and Bacillus amyloliquefaciens CHCC 15516 | 抗微生物(Antimicrobial) | 体外/细胞系(In vitro/cell lines) | 抑制肠致病性大肠杆菌F4、CHCC 15541介导的HT29-16E细胞中黏液基因MUC2和MUC3的表达。研究表明这些芽孢杆菌菌株具有抗病原性和益生特性(Bravo Santano等,2020) |
| Bacillus licheniformis, Bacillus subtilis | 抗微生物(Antimicrobial) | 体外/J774A小鼠细胞系(In vitro/J774A mouse cell line) | 利用益生菌Bacillus licheniformis开发微生物胞外陷阱(METs)作为控制致病性金黄色葡萄球菌的新策略(Romo-Barrera等,2021) |
| Bdellovibrio bacteriovorus | 抗微生物(Antimicrobial) | 体外(In vitro) | 可能作为益生菌使用(Dwidar等,2012;Bonfiglio等,2020;Cavallo等,2021),对抗生物膜形成的革兰氏阴性菌,抑制革兰氏阳性金黄色葡萄球菌。作为独特的特征,Bdellovibrio bacteriovorus通常抑制革兰氏阳性细菌(Kahraman Vatansever等,2023) |
| Butyricicoccus pullicaecorum 25-3ᵀ | 促进健康(Pro-health) | 体外/动物模型/人类(In vitro/animals, humans) | Butyricicoccus pullicaecorum 25-3ᵀ是首个被证实能产生丁酸盐的菌株,对哺乳动物和志愿者安全。包埋的Butyricicoccus pullicaecorum 25-3ᵀ在4 °C下稳定且具有活性长达8个月,在商业制剂中可保持稳定,因此可被视为一种潜在的下一代益生菌(Boesmans等,2018) |
| 对炎症性肠病(IBDs)患者安全(Steppe等,2014) | |||
| Butyricicoccus pullicaecorum | 抗癌作用(Anticancer) | 活体(In vivo) | 具有耐受低pH(pH 2.0和3.0)以及胆汁和胰液的能力,无不良反应,可产生短链脂肪酸(SCFAs),其介导的抗肿瘤活性包括诱导膀胱尿路上皮细胞凋亡(Chang等,2020;Wang等,2021) |
| Clostridium butyricum | 抗癌作用(Anticancer) | 小鼠模型(Apcmin/+小鼠)(In vivo/Apcmin/+ mice) | 抑制高脂饮食诱导的小鼠肠道肿瘤发生,减少肠道肿瘤细胞增殖,抑制Wnt/β-catenin信号通路,调节有益肠道菌群,增强SCFAs水平,并降低粪便中次级胆汁酸含量(Chen等,2020) |
| 神经保护作用(Neuroprotective) | 人类(肥胖人群)、小鼠模型(In vivo/humans, obese mice) | 肥胖人群中缺乏Clostridium butyricum。通过粪菌移植(FMT)和补充优质Clostridium butyricum菌株,可预防肠道微生物失调,改善肠道屏障功能和认知障碍(在小鼠模型中观察到)(Zheng等,2024) | |
| Clostridium tyrobutyricum | 预防腹泻(Prevention of diarrhea) | 小鼠模型(In vivo/mice) | 抑制LPS诱导的腹泻和结肠炎症,增强Th1细胞比例以响应LPS。其保护作用独立于SCFA的合成与作用(Xiao等,2021) |
| Dubosiella newyorkensis | 抗衰老作用(Antiaging effects) | 小鼠模型(In vivo/mice) | 具有降压、抗氧化、抗衰老和保肝特性。该细菌可促进肠道有益菌群生长,并预防与年龄相关的疾病(Liu等,2023) |
| Fecalibacterium prausnitzii | 改善肠道屏障(Improved intestinal barrier) | 体外/小鼠模型(人类克罗恩病)(In vitro/in vivo mice (models of human CD)) | F. prausnitzii 和丁酸盐合成菌(如 Butyricicoccus pullicaecorum 25-3ᵀ)可增强丁酸盐浓度达 5–11 mol%,提高微生物定植能力,并影响黏液层和腔内相关肠道菌群(Geirmart 等,2017) |
| Hafnia alvei HA4597® | 控制肥胖(Obesity control) | 高脂饮食喂养的小鼠肥胖模型(HFD-fed mice models of obesity) | 减少食欲和食物摄入,降低体重增加,因此可用于控制体重和肥胖(Legrand等,2020) |
| 小鼠肥胖模型(In vivo/mice models of obesity) | 给予小鼠1.4 × 10¹⁰ CFU的H. alvei HA4597连续38天,结果显示体重和脂肪质量增长减少,食物摄入量与标准饮食对照组相当。治疗动物血糖、血清总胆固醇和ALT水平均下降(Lucas等,2019) | ||
| 人体志愿者(In vivo/human volunteers) | 在服用H. alvei(每日1000亿细菌)12周后观察到:饱腹感增强、臀围减小,空腹血糖显著低于安慰剂或对照组(Déchelotte等,2021) | ||
| Weizmannia coagulans PL-W | 抗微生物、产生细菌素(Antimicrobial, Bacteriocins) | 体外(In vitro) | 从发酵食品中分离的该菌株基因组序列显示含有细菌素合成基因簇,以及与宿主细胞粘附相关的基因。其产生的细菌素对李斯特菌(Listeria monocytogenes)、枯草芽孢杆菌(Bacillus subtilis)和金黄色葡萄球菌(Staphylococcus aureus)具有拮抗作用(Wang 等,2023) |
| Weizmannia coagulans SANK70258 | 抗微生物(Antimicrobial) | 活体/肉鸡(In vivo/broilers) | 上调肠道免疫和屏障功能,减少肠道病变,刺激致病性梭状芽孢杆菌(Alitipes spp.)和肠球菌属(Enterococcus spp.)的生长抑制(Aida 等,2023) |
参考文献
1.Aida M, Yamada R, Nakamura SI, Imaoka T, Shimonishi H, Matsuo T, Taniguchi I, Tsukahara T (2022) The effect of supplementation with Weizmannia coagulans strain sank70258 to coccidia-infected broilers is similar to that of a coccidiostat administration. Vet Sci 9(8):406. https://doi.org/10.3390/vetsci9080406. PMID: 36006321
2.Cani PD, Depommier C, Derrien M, Everard A, de Vos WM (2022) Akkermansia muciniphila: paradigm for next-generation beneficial microorganisms. Nat Rev Gastroenterol Hepatol 19(10):625–637. https://doi.org/10.1038/s41575-022-00631-9. Online ahead of print. PMID: 35641786
3.Chen H, Qian Y, Jiang C, Tang L, Yu J, Zhang L, Dai Y, Jiang G (2024) Butyrate ameliorated ferroptosis in ulcerative colitis through modulating Nrf2/GPX4 signal pathway and improving intestinal barrier. Biochim Biophys Acta Mol Basis Dis 1870(2):166984. https://doi.org/10.1016/j.bbadis.2023.166984. Epub 2023 Dec 6. PMID: 38061600 References
4.Guo X, Li S, Zhang J, Wu F, Li X, Wu D, Zhang M, Ou Z, Jie Z, Yan Q, Li P, Yi J, Peng Y (2017) Genome sequencing of 39 Akkermansia muciniphila isolates reveals its population structure, genomic and functional diversity, and global distribution in mammalian gut microbiotas. BMC Genomics 18(1):800. https://doi.org/10.1186/s12864-017-4195-3. PMID: 29047329
5.Sreenadh M, Kumar KR, Nath S (2022) In vitro evaluation of Weizmannia coagulans strain LMG S-31876 isolated from fermented Rice for potential probiotic properties, safety assessment and technological properties. Life (Basel) 12(9):1388. https://doi.org/10.3390/life12091388. PMID: 36143423
6.Zheng M, Ye H, Yang X, Shen L, Dang X, Liu X, Gong Y, Wu Q, Wang L, Ge X, Fang X, Hou B, Zhang P, Tang R, Zheng K, Huang XF, Yu Y (2024) Probiotic Clostridium butyricum ameliorates cognitive impairment in obesity via the microbiota-gut-brain axis. Brain Behav Immun 115:565–587. https://doi.org/10.1016/j.bbi.2023.11.016. Epub 2023 Nov 17. PMID: 379810127 Non-lactic Acid Bacteria and Other Novel Probiotics
相关产品
HZB205362:布拉酵母菌 | Saccharomyces Boulardii
HZB719577:普拉梭菌 | Faecalibacterium prausnitzii
HZB487452:嗜黏蛋白阿克曼菌 | Akkermansia muciniphila
HZB218990:芽孢杆菌属 | Bacillus sp.
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-03-05
编制人:思琪
审稿人:小藻
