合成生物学核心驱动力:底盘细胞(大肠杆菌与酿酒酵母)的深度解析与工业应用
来源:武汉市灰藻生物科技有限公司 浏览量:309 发布时间:2026-02-28 14:10:36
一、引言
合成生物学(Synthetic Biology)的核心理念是将工程学原则应用于生命科学,通过“自下而上”的方式设计、改造甚至从头合成生物系统。
在这一跨学科领域中,底盘细胞(Chassis cells)扮演着极其关键的角色,它们是承载人工设计基因回路、代谢途径和各类生物模块的“硬件平台”。
随着全球由化石经济向生物经济(Bio-economy)转型,传统化工合成面临高耗能、高污染的困境。
利用微生物作为细胞工厂(Cell factories)进行生物制造,已成为生产医药、高价值精细化学品、大宗化学品及生物燃料的可持续替代方案。
理想的底盘细胞必须具备遗传背景清晰、生长快速、易于进行基因操作、代谢网络可塑性强以及工业发酵放大表现稳定等特质。
经过数十年的研究与工业化筛选,原核生物中的大肠杆菌(Escherichia coli)与真核生物中的酿酒酵母(Saccharomyces cerevisiae)脱颖而出,成为目前合成生物学中最经典、应用最广泛的两大底盘细胞平台。
二、底盘细胞的设计原则与改造机制
天然微生物的进化目的是为了自身的生存和繁衍,而非为人类高效合成特定化学品。因此,将野生型菌株转化为高效的工业底盘细胞,需要进行深度的基因组与代谢网络重编程。
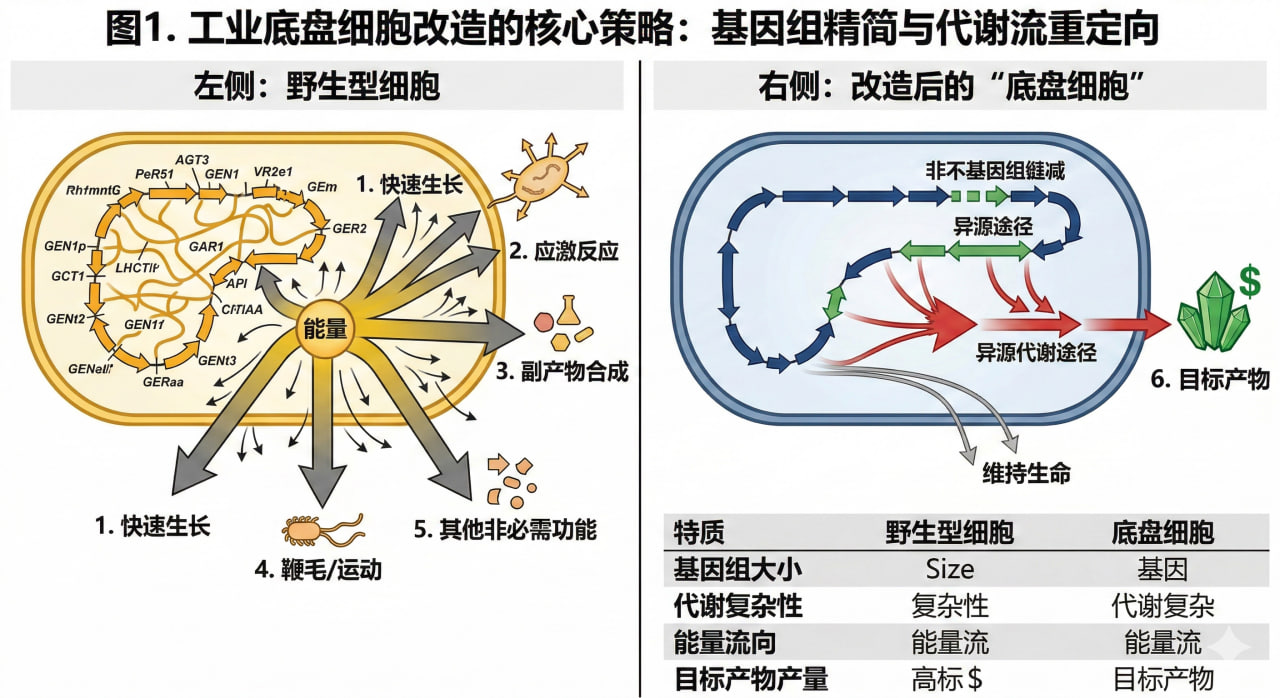
图1. 工业底盘细胞改造的核心策略:基因组精简与代谢流重定向
2.1 基因组精简(Genome Reduction)
野生菌株基因组中存在大量冗余基因(如原噬菌体、插入序列、非必需代谢途径基因等),这些基因不仅消耗细胞代谢能量,还可能引发基因组不稳定性。
通过敲除这些非必需片段,可以构建出“最小基因组底盘”。精简后的底盘细胞通常表现出更高的外源基因表达效率、更快的生长速率以及更少的内源代谢物干扰。
2.2 代谢通路重构与辅因子平衡
高产底盘细胞需要强大的前体物供应和能量代谢平衡。改造机制主要包括解除变构抑制与碳代谢物阻遏,突变关键限速酶的调控位点,使代谢流能够无阻碍地流向目标产物。
同时,辅因子工程(Cofactor Engineering)也是提升产率的核心,通过重构跨膜电子传递链或引入异源辅因子再生系统,维持细胞内氧化还原(如 NADH/NAD⁺)平衡。
三、原核底盘代表:大肠杆菌(E. coli)
大肠杆菌是人类研究最透彻的模式生物,其作为原核底盘在合成生物学中占据着不可撼动的“主力军”地位。
3.1 生物学特性与核心优势
大肠杆菌具有极短的生长周期(在 LB 培养基中对数期倍增时间仅需 20-30 分钟),能够在短时间内积累极高的生物量。其外源基因表达系统极为成熟,拥有庞大的启动子库(如 T7、trc、pBAD 等)和质粒载体系统。
此外,它能在简单的无机盐培养基上利用多种碳源(葡萄糖、甘油、木糖等)高效生长,极大降低了工业发酵的原料成本。
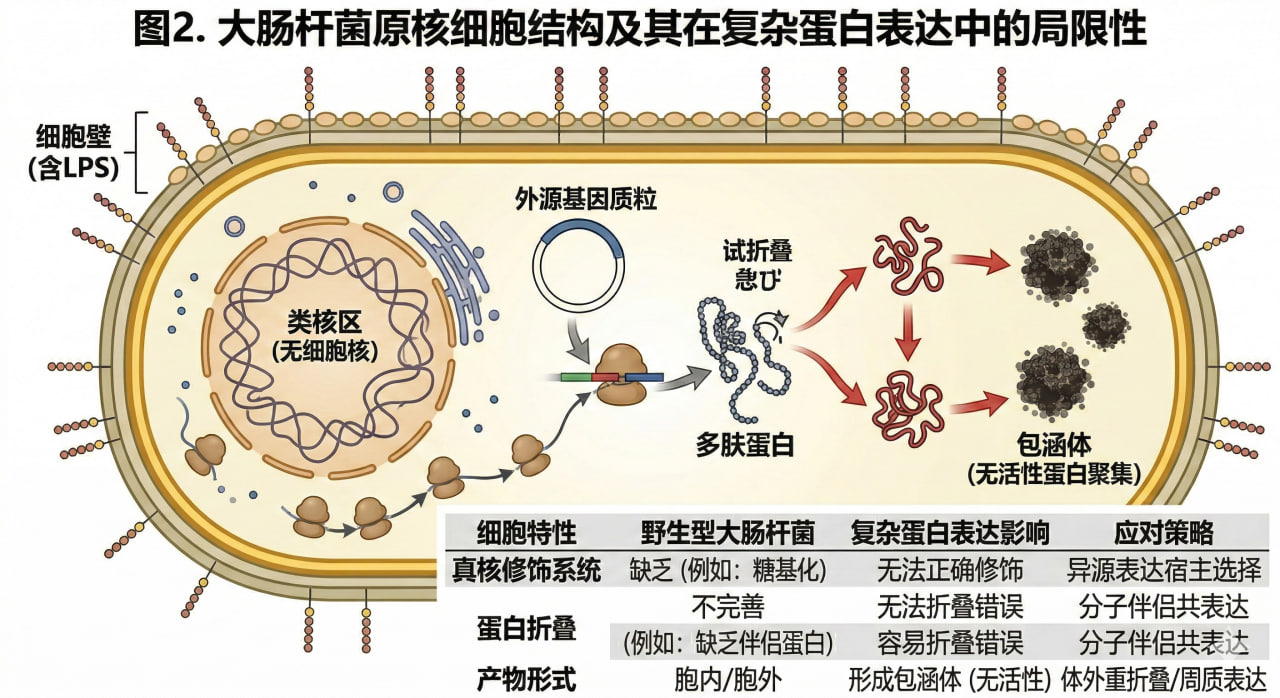
图2. 大肠杆菌原核细胞结构及其在复杂蛋白表达中的局限性
3.2 常见工程衍生菌株与应用局限
工业界开发了多种针对性底盘:如用于质粒扩增的 DH5α(缺失 recA1 和 endA1),以及专门用于蛋白表达的 BL21(DE3)(缺失 Lon 和 OmpT 蛋白酶)。
然而,大肠杆菌最大的劣势在于缺乏真核生物的内膜系统,无法对表达的复杂蛋白进行翻译后修饰(Post-translational modifications, PTMs),如糖基化。
此外,其细胞壁含有的脂多糖(LPS,即内毒素)也限制了其在医用注射药物中的应用。
四、真核底盘代表:酿酒酵母(S. cerevisiae)
针对大肠杆菌在复杂化合物和高级蛋白合成上的短板,酿酒酵母作为最基础的真核底盘,提供了完美的解决方案。
4.1 真核内膜系统的优势
酿酒酵母被 FDA 认定为 GRAS(一般认为安全) 级别的微生物。它拥有与高等动植物高度相似的内膜系统(内质网、高尔基体),能够完成外源蛋白的信号肽切除、折叠、二硫键配对以及高度复杂的糖基化修饰,是生产抗体、人血清白蛋白等高端医药蛋白的理想宿主。
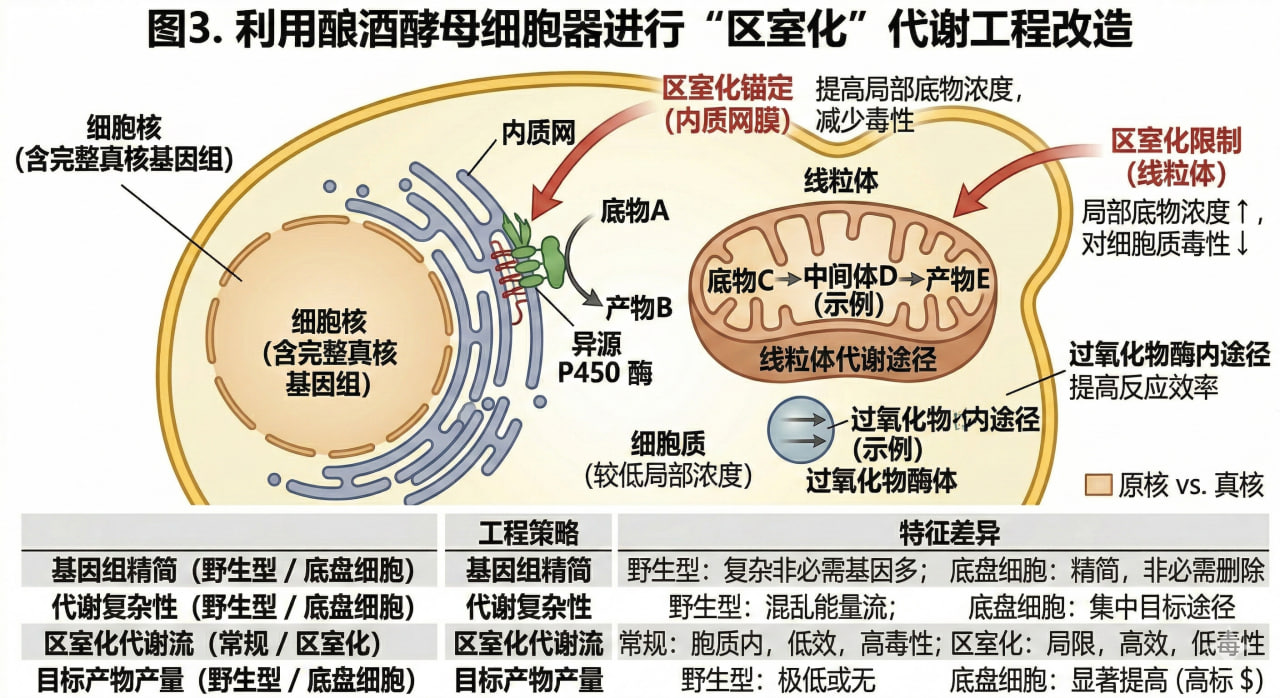
图3. 利用酿酒酵母细胞器进行“区室化”代谢工程改造
4.2 天然产物合成的“明星底盘”
酿酒酵母拥有极高的同源重组效率,利于大片段基因簇的染色体整合。同时,它天然拥有丰富的甲羟戊酸途径(MVA pathway)代谢流,是合成萜类化合物(如青蒿素、番茄红素、紫杉醇前体)的绝佳宿主。
五、影响底盘细胞发酵效率的关键因素
无论底盘细胞在实验室摇瓶阶段表现多么优异,在进入工业级发酵罐时,仍会受到多重环境与生化因素的制约。
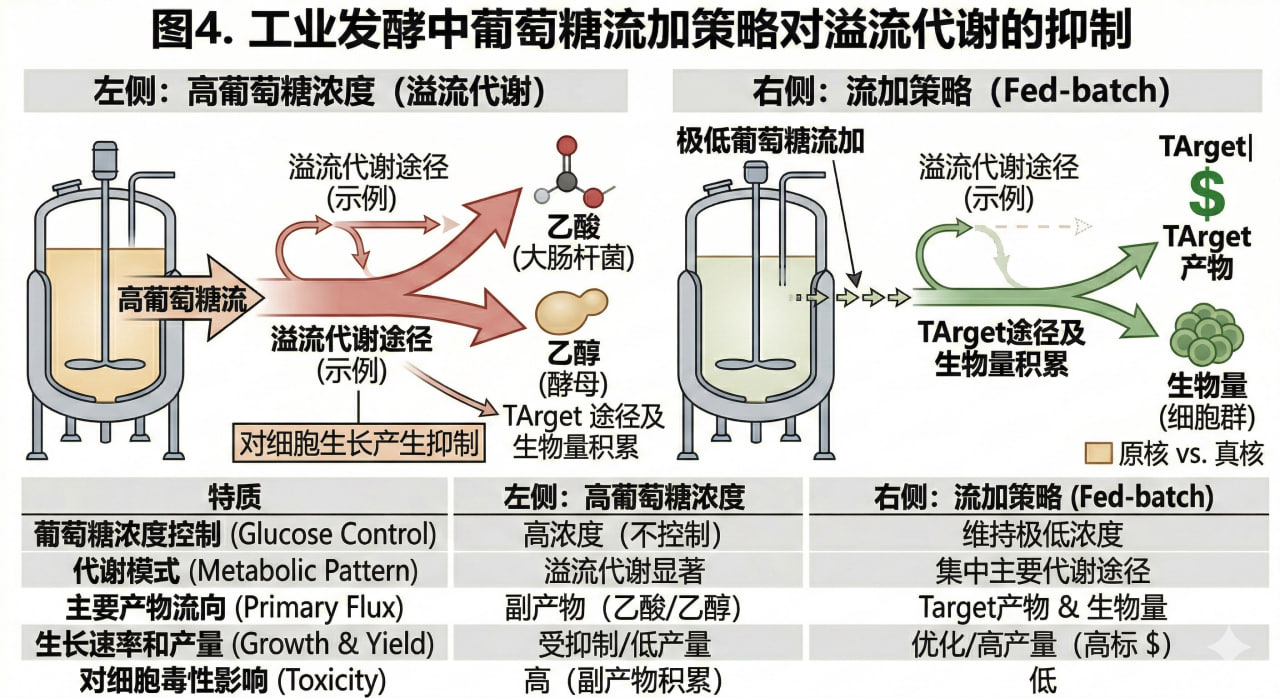
图4. 工业发酵中葡萄糖流加策略对溢流代谢的抑制
5.1 营养供给与“溢流代谢”
过高的碳源浓度会引发大肠杆菌的“溢流代谢”(Overflow metabolism),生成大量乙酸副产物。在工业发酵中,必须采用流加策略(Fed-batch),严格控制补料速率,维持极低的胞外底物浓度。
5.2 溶氧与环境参数
多数需氧型底盘细胞的高效运转高度依赖氧气。大肠杆菌最适生长温度在 37°C,pH 在 6.8-7.2;而酿酒酵母最适温度在 28-30°C,其卓越的耐酸性(可运行在 pH 4.0-5.5)有效降低了工业发酵中杂菌污染的风险。
六、底盘细胞的工业实际应用对比
经过理性设计与多轮改造,大肠杆菌与酿酒酵母底盘细胞已在医药、化工、食品等多个领域实现了颠覆性的产业化应用(表1)。
表1. 大肠杆菌与酿酒酵母底盘在工业生物制造中的典型应用对比
| 目标产物分类 | 典型产物 | 优选底盘细胞 | 作用机制与底盘优势 |
|---|---|---|---|
| 生物医药蛋白 | 人胰岛素(Insulin) | 大肠杆菌(E. coli) | 表达量极大,成本极低。早期的标志性生物技术成果。 |
| HPV疫苗(VLP)、抗体片段 | 酿酒酵母(S. cerevisiae) | 需高级结构正确折叠与适度糖基化。酵母底盘更安全、有效。 | |
| 高价值天然产物 | 透明质酸(Hyaluronic acid) | 大肠杆菌(E. coli) | 重构简单合成途径,敲除竞争路径。原核体系操作周期短。 |
| 青蒿酸、人参皂苷 | 酿酒酵母(S. cerevisiae) | 引入植物源复杂 P450 酶系。酵母拥有内质网膜,可锚定 P450 酶。 | |
| 大宗化学品与有机酸 | 1,4-丁二醇 (BDO)、丁二酸 | 大肠杆菌(E. coli) | 重构厌氧和 TCA 循环途径,实现碳原子高转化率。 |
| 长链二元酸、乳酸 | 酿酒酵母(S. cerevisiae) | 酵母耐低 pH,发酵过程无需大量碱中和,简化下游纯化。 |
七、未来方向:从“试错”走向“理性设计”
随着遗传工具的爆发,底盘细胞的开发正迎来新的变革:
- CRISPR/Cas 多位点编辑:实现全基因组水平的同步敲除或整合。
- 非模式底盘崛起:如利用甲醇的毕赤酵母、利用废塑料的盐单胞菌。
- 人工智能辅助设计(AI & ML):利用深度学习模型预测蛋白质结构(如 AlphaFold)和推演最佳发酵策略。

- 图5. 合成生物学工程化循环:Design-Build-Test-Learn (DBTL)
八、结论
大肠杆菌与酿酒酵母作为合成生物学时代的基石,分别在原核和真核维度展现出了无与伦比的工程学潜力。通过深入理解底盘细胞的代谢机制并融合前沿的人工智能技术,精心雕琢的细胞工厂将引领新一轮的“绿色工业革命”,为解决全球资源枯竭和环境污染问题提供可持续的生物基方案。
参考文献
1. Keasling, J. D. (2010). Manufacturing molecules through metabolic engineering. Science, 330(6009), 1355-1358.
2. Ro, D. K., et al. (2006). Production of the antimalarial drug precursor artemisinin in engineered yeast. Nature, 440(7086), 940-943.
3. Yim, H., et al. (2011). Metabolic engineering of Escherichia coli for direct production of 1,4-butanediol. Nature Chemical Biology, 7(7), 445-452.
4. 连佳长, 等. (2018). 合成生物学底盘细胞的构建与应用研究进展. 生物工程学报, 34(8), 1223-1234.
相关产品
HZB208299:EBY100 酿酒酵母 Competent Cells
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-02-27
编制人:小段
审稿人:小藻
