微生物生长动力学:标准化生长曲线构建与代谢物分析
来源:武汉市灰藻生物科技有限公司 浏览量:315 发布时间:2026-02-28 14:54:30
一、引言
在生命科学研究与工业发酵领域,微生物生长动力学(Microbial Growth Kinetics)是理解细胞代谢规律、优化培养工艺的基石。
无论是评估新型抑菌剂的效价,还是开发高效的细胞工厂,绘制一条精确的微生物生长曲线并同步监测其代谢物变化,都是不可或缺的核心环节。
一个标准化的生长实验,不仅要求对菌株背景有清晰的认知,更需要极高的实验设计严谨度。
从标准保藏库获取菌株的活化,到分光光度法(OD600)的精准测量,再到复杂代谢物在不同生长阶段的动态收集,每一个步骤都直接决定了最终数据的可重复性与科学价值。
本文将系统性地,拆解微生物标准化生长曲线的构建流程,深入探讨关键时间点的取样策略、OD测量误差的规避方法,以及如何在特定培养条件(如厌氧环境)下,进行高效的代谢物动力学分析。
二、菌株溯源与前期复苏准备
一切严谨的动力学实验,都始于对目标微生物的准确分类与标准化复苏。在开展正式的生长曲线测定前,确保菌种的纯度与活力是重中之重。
2.1 标准参考菌株的获取
为了保证实验结果具备全球可比性,研究人员通常会从权威的微生物保藏中心(如德国微生物菌种保藏中心 DSMZ 或美国 ATCC)获取标准参考菌株。
了解目标菌株具体的生理生化特性,是配置最适培养基(如特定碳氮比、微量元素补充)的前提。
2.2 梯次活化与种子液制备
保藏状态下的菌株(如甘油管冻存或冷冻干燥粉)通常处于深度休眠期。直接将其接种用于生长曲线测定会导致极长且不稳定的延滞期(Lag phase)。
标准操作流程要求至少进行两次梯次活化:
首先在固体平板上划线分离单菌落以验证纯度,随后挑取形态饱满的单菌落接种至液体培养基中,培养至对数生长期中后期(OD600 约为 0.6-0.8),作为最终的种子液(Seed culture)进行统一接种。
三、标准化生长曲线的构建策略
微生物在封闭系统(分批培养)中的生长通常遵循四个经典阶段:延滞期、对数期(指数期)、稳定期和衰亡期。
为了精确描绘这一动态过程,实验设计必须兼顾统计学严谨与时间维度的连续性。
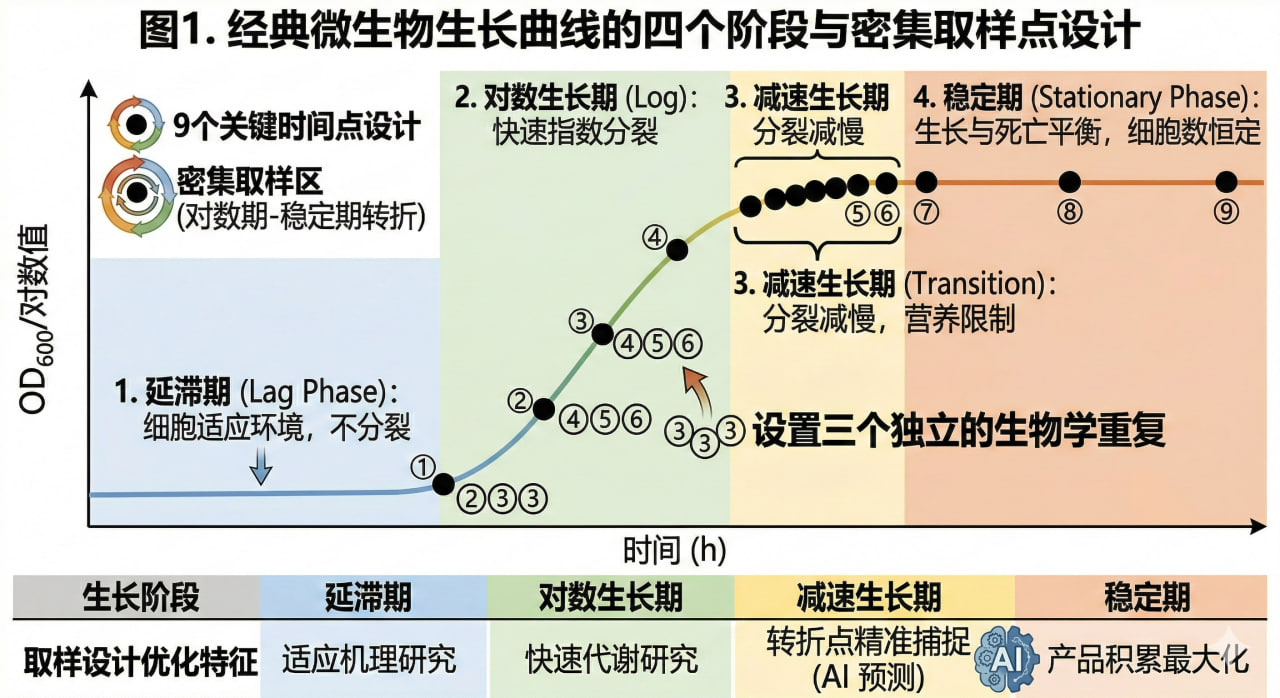
图1. 经典微生物生长曲线的四个阶段与密集取样点设计
3.1 三生物学重复与接种同步化
为消除个体差异和操作误差对生长的影响,一个高质量的动力学实验强制要求设置三个独立的生物学重复(Triple duplicates)。
接种时,必须确保初始接种量(通常为 1% - 5% v/v)绝对一致,且将培养体系的初始 OD600 统一调整至同一基准线(如 0.05),以确保所有摇瓶或培养管同步起跑。
3.2 科学的密集时间点取样
时间跨度的设定依赖于菌株的世代时间(Generation time)。为了精准捕捉代谢发生剧变的转折点(尤其是对数期末期向稳定期过渡的阶段),实验往往需要设定密集的取样频率。
以常规细菌为例,通常会精密设定9个关键时间点(如 0h, 2h, 4h, 6h, 8h, 10h, 12h, 16h, 24h)进行持续追踪。这种高密度的取样策略是后续代谢物动力学拟合的数据基础。
四、OD600 分光光度法的操作陷阱与校准
吸光度测量(Optical Density at 600 nm, OD600)是目前最常用、最便捷的生物量宏观表征手段,但其本质是测量细胞悬液对光线的散射(Scattering),而非吸收。
4.1 线性范围与梯度稀释
分光光度计仅在特定的低浓度区间内,OD值才与细胞浓度呈严格的线性关系(比尔-朗伯定律的近似应用)。
当培养液的 OD600 超过 0.6 或 0.8(取决于具体仪器)时,由于严重的“二次散射”效应,测得的数值会显著低于真实生物量。
因此,在对数期和稳定期取样时,必须使用无菌培养基对样本进行适当倍数的梯度稀释,使测量值回落至 0.2 - 0.6 的线性安全区内,最后再乘以稀释倍数计算真实 OD 值。
4.2 空白对照与基质扣除
在长达数十小时的培养过程中,培养基本身的颜色可能会因氧化、酸碱度改变或代谢物分泌而加深。
必须在每一个取样时间点,使用与发酵液经历同等温度与震荡条件、但未接种的纯培养基作为空白对照(Blank)进行调零,以彻底排除背景干扰。
五、关键代谢物的动态收集与分析
生长曲线描绘的是细胞“量”的积累,而同步进行的代谢物分析则揭示了细胞内部“质”的变化。这两者的拟合,是解析微生物物质代谢流向的关键。
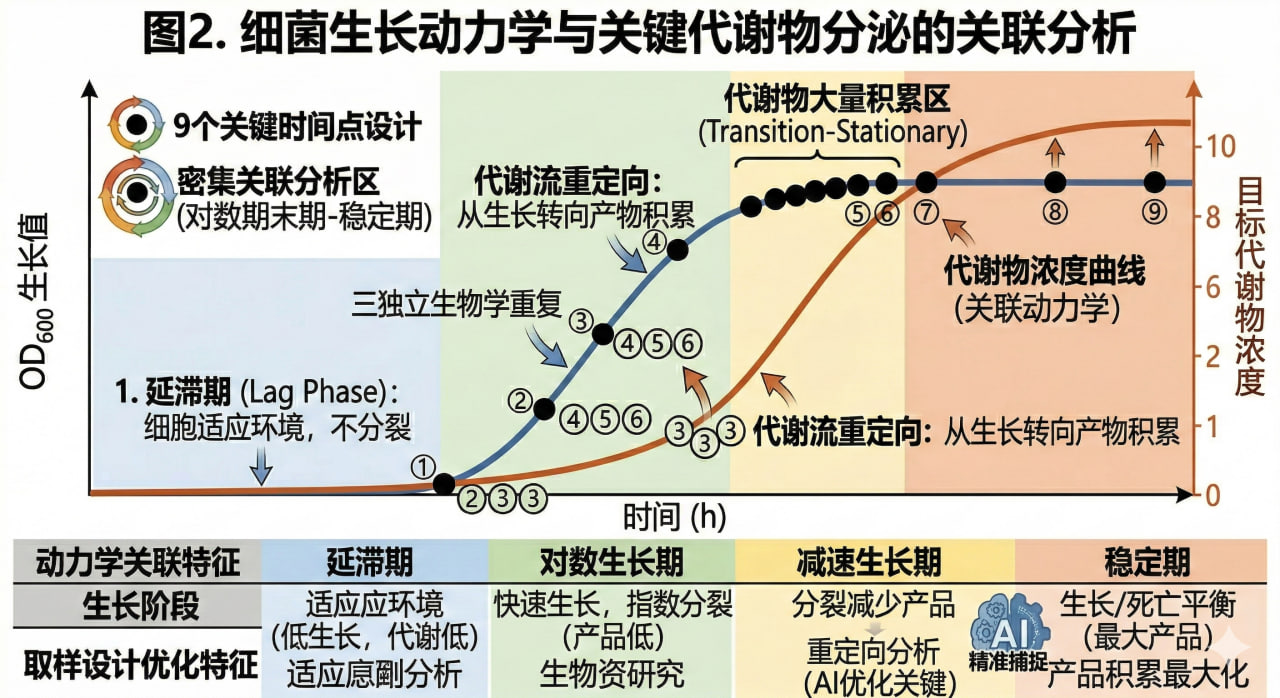
图2. 细菌生长动力学与关键代谢物分泌的关联分析
5.1 代谢物的分类与截留策略
根据生成规律,微生物代谢产物可分为:
- 初级代谢产物(Primary metabolites):如氨基酸、核苷酸等,其合成曲线通常与细胞生长曲线高度平行(偶联型)。
- 次级代谢产物(Secondary metabolites):如抗生素、毒素、色素等,往往在细胞进入稳定期,面临营养耗尽和生存压力时才开始大量合成(非偶联型)。
在前述设定的 9 个时间点取样时,不仅要测量 OD,还需同步将菌液离心。
上清液需立即经 0.22 μm 滤膜过滤后冻存于 -80°C,用于后续的 HPLC(高效液相色谱)或 GC-MS 分析;而细胞沉淀则常用于胞内酶活力的测定或转录组学提取。
5.2 厌氧培养(Anaerobic Cultivation)下的代谢分流
值得特别注意的是,环境中的溶解氧(DO)是调控代谢流向的“主开关”。在进行厌氧培养时,微生物(如兼性厌氧菌)无法通过氧化磷酸化获取能量,其代谢途径会发生剧烈分流,转向混酸发酵或特定的还原途径。
此时,原本可能大量积累的生物量(OD值)会显著下降,取而代之的是乳酸、丁二酸等特定有机酸在培养基中的大量分泌。因此,在评估无氧条件下的生长动力学时,代谢物浓度的监测往往比单纯的 OD 测量具有更高的指导意义。
六、常见技术问题与排障指南
在长周期的动力学实验中,研究者常会遭遇各种导致曲线“畸形”的状况,表1列举了最常见的问题及应对策略。
| 异常现象 | 可能原因分析 | 优化与排障建议 |
|---|---|---|
| 延滞期(Lag phase)异常漫长 | 1. 种子液老化或处于衰亡期; 2. 接种量过低(< 1%); 3. 培养基成分与活化基质差异过大。 | 确保种子液处于对数中后期;统一采用 2%-5% 接种量;活化与发酵使用同源配方培养基。 |
| 对数期(Log phase)提前结束,最终 OD 偏低 | 1. 关键营养元素(碳源、氮源或特定维生素)过早耗尽; 2. 代谢酸性产物积累导致 pH 剧降。 | 检测残糖含量;在培养基中加入足够的缓冲盐体系(如磷酸缓冲液)维持 pH 稳定。 |
| 高密度阶段 OD 测量值出现波动或假性下降 | 1. 未进行梯度稀释,超出仪器线性范围; 2. 菌体发生自溶或相互聚集成团块。 | 严格执行高浓度样本稀释;测量前充分震荡混匀,必要时可加入微量表面活性剂分散菌落。 |
七、总结
构建标准的微生物生长动力学曲线并不仅是按时记录几个数值,它是一项系统性的分析工程。从严守 DSMZ/ATCC 菌株的生理特性,到设计包含三重复与 9 个密集取样点的严密流程;
从规避分光光度法的光学陷阱,到揭示厌氧培养下代谢物分流的深层逻辑,每一步都凝聚着生命科学研究的严谨与精妙。
掌握这套标准化的动力学分析方法,研究人员便能更清晰地透视细胞工厂的运行轨迹,从而为发酵工艺的优化、新型生物材料的合成以及疾病致病机制的解析提供最坚实的数据支撑。
参考文献
1. Monod, J. (1949). The growth of bacterial cultures. Annual Review of Microbiology, 3(1), 371-394.
2. Maier, R. M. (2009). Bacterial growth. In Environmental Microbiology (pp. 37-54). Academic Press.
3. Pirt, S. J. (1975). Principles of microbe and cell cultivation. Blackwell Scientific Publications.
相关产品与服务
敬请关注灰藻生物,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共创生命科学的美好未来!
更新日期:2026-02-27
编制人:小段
审稿人:小藻
