文章综述 | 人类肠道微生物组成及其在疾病早期诊断中的意义
来源:武汉市灰藻生物科技有限公司 浏览量:1417 发布时间:2024-12-11 22:10:16
引言
近年来,肠道微生物与人类健康的关系成为一个日益增长的研究领域。胃肠道微生物通过复杂的网络相互连接,形成了所谓的肠-微生物-脑轴,这种关系可能对大脑和脊髓(即中枢神经系统)的健康和疾病有着重要影响。微生物和中枢神经系统通过自主神经、神经内分泌、胃肠道和免疫系统路径双向互动。肠道微生物已与多种胃肠道内外的疾病联系起来。由于分子工具和技术(如宏基因组学、代谢组学、脂质组学、宏转录组学)的发展,宿主和不同微生物之间发生的复杂相互作用正逐步被破译。最新的研究表明,肠-微生物-脑轴可能在包括抑郁症、痴呆症、创伤后应激障碍、焦虑症、双相情感障碍、精神分裂症和强迫症等神经精神障碍中扮演角色,同时也涉及诸如肥胖、糖尿病和炎症等慢性宿主疾病。
人类身体被各种细菌及其代谢产物定植,其中肠道拥有最大的微生物群。人体肠道微生物是由100万亿细菌、病毒、真菌和古菌组成的复杂生态系统,它与宿主共同进化。饮食、生活方式、遗传以及婴儿期都会影响肠道微生物的构成。肠道微生物的多样生物,在维持人类健康方面发挥着重要作用,例如通过分解食物释放人体无法获得的营养,促进宿主细胞分化,防止病原体定植,以及增强或调节免疫系统。一些胃肠道疾病,如肠易激综合症、乳糜泻、结肠癌、慢性肝病和胰腺问题,一直是深入研究肠道微生物重要性的焦点。研究还指出,肠道微生物可能是包括抑郁症、阿尔茨海默病、痴呆症、创伤后应激障碍、焦虑症、双相情感障碍、精神分裂症和强迫症在内的,心理健康问题的潜在生物标志。肠道微生物参与免疫、能量、脂质和糖代谢的多种途径影响。
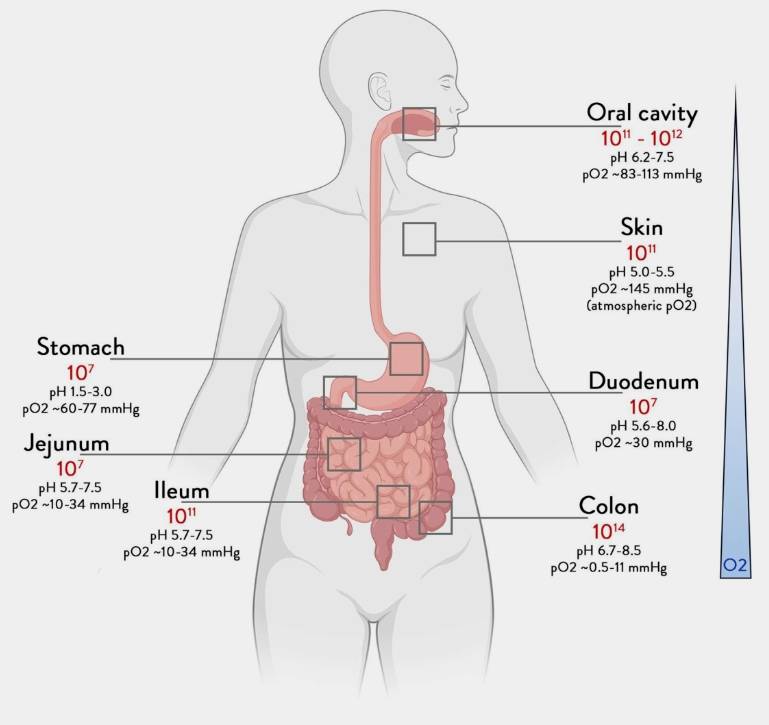
人体肠道微生物(图源:GUT期刊)
人类微生物群基因和产物自出生以来就在我们的身体上定居,并垂直转移。虽然所有身体部位都被微生物定殖,但在肠道中发现的微生物数量最多。使用“慢性肝病”、“结直肠癌”、“乳糜泻”、“肠易激综合征”、“抑郁症”、“焦虑症”、“乳腺癌”、“精神分裂症”、“阿尔茨海默病”、“胃肠道微生物”作为关键词,分析了1999-2023年的PUBMED中88篇相关文章,总结了其中关于肠道微生物的相关描述。人类口腔和唾液微生物组包含数以百万计的微生物,它们在肠道中的持久性受到许多因素影响,如胃酸度,胆汁酸(BAs)、消化酶和抗菌蛋白等。pH值、氧浓度和氧化还原电位、粘液等化学参数,以及肠道结构、蠕动和转运时间等物理方面也会影响。小肠中每单位含有数千到数亿个细胞,其中部分耐氧的厚壁菌门(Firmicutes)和变形菌门(Proteobacteria)是主要的门。结肠中的转运时间比在小肠中的转运时间要长十几倍,每单位细菌数量更加丰富。结肠微生物群以厌氧细菌为主,主要为厚壁菌门(瘤胃球菌科Ruminococcaceae和毛螺菌科Lachnospiraceae)、拟杆菌门(Bacteroidetes)、放线菌门(Actinobacteria)、变形菌门(Proteobacteria)和疣微菌门的阿克曼氏菌属(Akkermansia)。
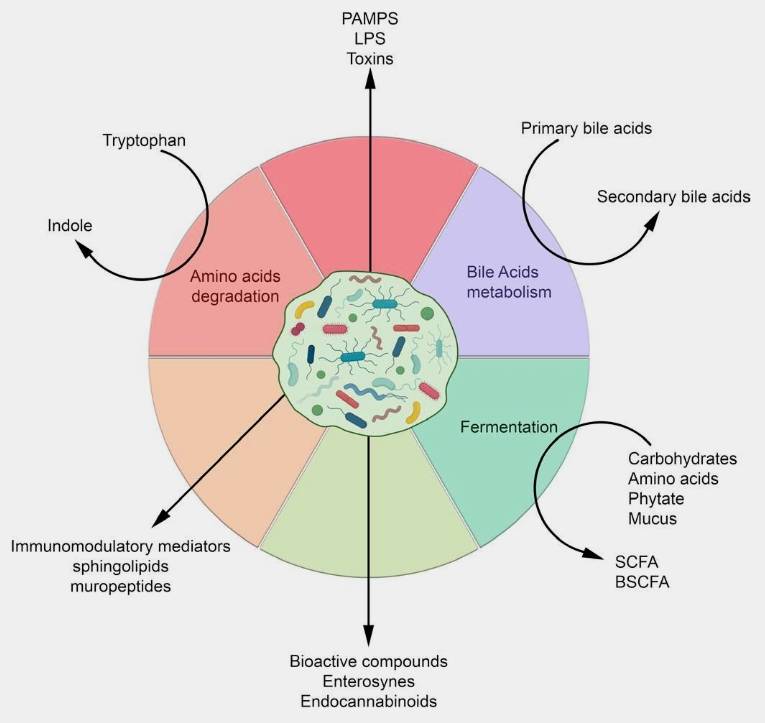
人体肠道微生物(图源:GUT期刊)
神经疾病与肠道微生物
阿尔茨海默病(AD)是一种神经退行性疾病,其病理生理学目前仍不完全清楚。多项研究表明,肠道微生物在AD发病机制中扮演了一定角色。阿尔茨海默病患者中,幽门螺杆菌(Helicobacter pylori)感染会导致炎症,并影响精神状态检查。此外,幽门螺杆菌及其他微生物(包括肺炎衣原体和伯氏疏螺旋体)感染的患者血液中A-40和A-42水平更高。这些微生物可能会相互作用,增加感染。在阿尔茨海默病患者的大脑海马区和颞叶脑裂解物中,发现了高量的细菌脂多糖。
患有脑淀粉样变性和认知障碍的人群血样中,也观察到了促炎细胞因子水平升高,同时抗炎大肠杆菌(Escherichia rectale)减少,促炎大肠杆菌/志贺氏菌(Escherichia/Shigella)增加。给大鼠注射氨苄西林后,导致血液皮质酮水平上升,焦虑行为增多。有趣的是,氨苄西林引起的身心异常,可以通过注射发酵乳杆菌(Lactobacillus fermentum NS9)来逆转。
抑郁症是最常见的精神疾病之一,研究表明,肠道微生物、D-氨基酸、短链脂肪酸和微生物代谢产物的变化,在抑郁症的发病机制中起着重要作用,同时也影响免疫系统和神经系统。粪便细菌与抑郁症间存在关联,抑郁症患者的肠道微生物失衡与较低的脑源性神经营养因子(BDNF)水平有关。整体肠道生态,包括50种粪便代谢物、47种细菌种类和3种噬菌体,在健康受试者和抑郁症患者之间有显著差异。布劳特氏菌属(Blautia sp)、颤杆菌属(Oscillibacter spp.)、瘤胃球菌属(Ruminococcus spp. 5_1_39BFAA),在患者体内的变化可能是抑郁症的重要指标。双歧杆菌科(Bacteroidaceae)水平的显著改变主要导致抑郁症,而类风湿球菌科(Ruminococcaceae)、普雷沃氏菌科(Prevotellaceae)和毛螺菌科(Lachnospiraceae)主要引起双相情感障碍。放线菌门(Actinobacteria)和厚壁菌门(Firmicutes)在抑郁症患者中非常普遍。在显著抑郁症患者中,研究显示布劳特氏菌(Blautia)与双歧杆菌(Bifidobacterium)数量增加,而普雷沃氏菌(Prevotella)数量减少。一项荟萃分析发现,益生菌干预疗法可以减轻抑郁症的症状,抑郁症患者的隐球菌(Cryptococcus)和粪便细菌水平低于非抑郁症对照组。
对肠道微生物组的调查,揭示了多达23个与抑郁症和焦虑症相关的微生物靶点。在抑郁症患者中,霍尔德曼氏菌(Holdemania)存在轻微联系。
双向情感障碍患者间,也观察到类似的肠道菌群变化。与未患病的人相比,黄杆菌(Flavonifractor)更为常见。
精神分裂症患者会出现幻觉、妄想和通常言语混乱等精神病症状。患之前的研究显示,放线菌门(Actinobacteria),与精神分裂症有正向因果关系,而β变形菌门(Betaproteobacteria)则其有积极影响。例如,普雷沃氏菌科(Prevotellaceae)产生的丙酸,被证明与感觉运动功能障碍、认知缺陷、社会异常以及自闭症谱系障碍症状加重有关。
粪杆菌(Faecalibacterium)降低,可能导致精神分裂症患者肠道TH17细胞增加。据推测,这些细胞可能穿过血脑屏障并刺激海马体的小胶质细胞,导致异常行为。韦荣球菌科(Veillonellaceae)和毛螺菌科(Lachnospiraceae),与精神分裂症患者疾病严重程度有关。与健康对照组相比,首次出现精神病发作的患者中乳杆菌科(Lactobacillaceae)发生了变化。另一项研究表明,接受利培酮或奥氮平治疗的患者与对照组相比,毛螺菌科(Lachnospiraceae)、阿克曼氏菌(Akkermansia)和萨特氏菌(Sutterella)的数量不同。
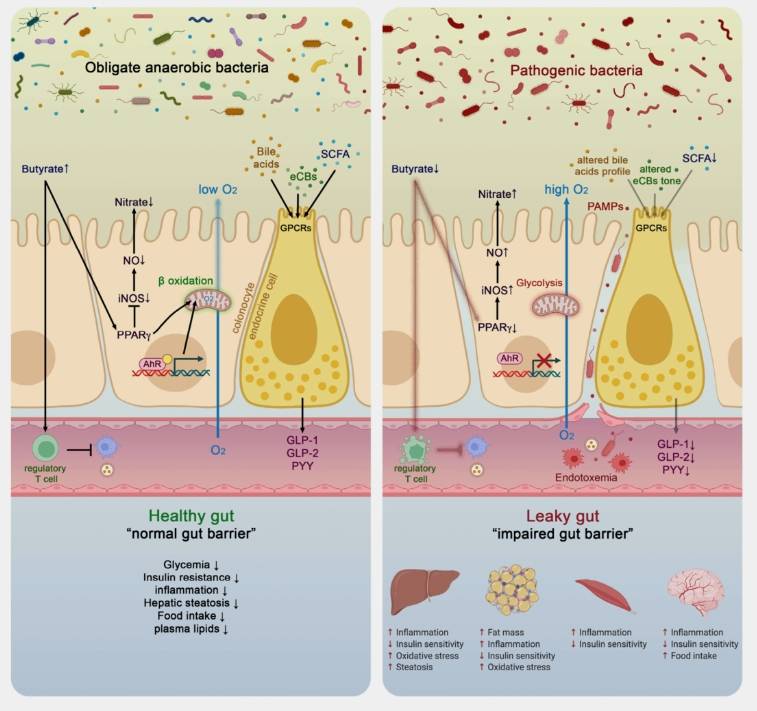
人体肠道微生物(图源:GUT期刊)
肠道疾病与肠道微生物
肠易激综合征(IBS)被认定为微生物-肠道-大脑轴功能失调的表现,IBS特征是反复出现的腹痛和排便频率或形态变化。2019年的一项研究表明,与健康对照组相比,IBS患者体内拟杆菌科(Bacteroidales)、乳酸菌科(Lactobacillaceae)以及肠杆菌科(Enterobacteriaceae)的数量较多,而双歧杆菌(Bifidobacterium)、粪杆菌(Faecalibacterium)和梭菌属(Clostridiales)的数量较低。此外,IBS患者的乙状结肠黏膜相关细菌组成也有所不同。
乳糜泻(CD)是一种慢性免疫疾病,其特点是对膳食蛋白麸质不耐受。一项研究使用16S rRNA测序,报告新生儿患者中乳酸杆菌(Lactobacillus)增加。
肠道菌群失调与结直肠癌(CRC)常常联系在一起。脆弱拟杆菌(Bacteroides fragilis)、具核梭杆菌(Fusobacterium nucleatum, Fn)和大肠杆菌(Escherichia coli)在CRC中扮演着重要角色。
在一小部分CRC患者中,通过荧光原位杂交技术发现了肿瘤内存在的具核梭杆菌序列。基于16S rRNA的CRC检查发现,革兰氏阳性纤维发酵型梭菌减少,粪便中的细菌多样性减少,口腔共生菌如具核梭杆菌(Fn)和卟啉单胞菌(Porphyromonas)增多。此外,Fn的增加与牙周病有关,这会增加CRC的风险。
粘附于粘膜的大肠杆菌(Escherichia coli)在CRC组织中更为常见,并且与癌症的分期和预后相关。当ApcMin/+小鼠被一种与结肠癌相关的E. coli菌株定植时,息肉的发生率显著增加,这表明某些E. coli菌株可能会促进致癌作用。
单剂量的霍氏厌氧丁酸菌(Anaerobutyricum hallii 或 ubacterium hallii) ,其使再生胰岛蛋白1B基因在十二指肠的表达水平增加了近10倍,还增加了代谢综合征受试者的血清胰高血糖素样肽-1(GLP-1)和次级胆汁盐,这可能解释了他们对葡萄糖反应的改善。
肝脏是外周器官和肠道循环血液汇聚的器官,肠道细菌对慢性肝病有着影响。研究表明,肠道微生物的变化可能是非酒精性脂肪肝发生的一个关键因素。在严重的酒精性肝炎(AH)中,微生物可能特别重要。首次描述了不同组别AH患者的肠道微生物,指出与AH相关的菌群失调以双歧杆菌(Bifidobacteria)、肠杆菌(Enterobacteria)和链球菌(Streptococci)的增加为标志。相反,某些物种,如抗炎菌株——粪普雷沃菌(Faecalibacterium prausnitzii)、(Clostridium clostridiforme)腐败梭菌(Clostridium septicum),则有所减少。肝硬化组中变形虫和梭杆菌数量增加,而拟杆菌门(Bacteroidetes)则显著减少。
乳腺组织的微生物群是独特的,除了乳头抽吸液和肠道微生物之外,某些物种还在乳腺组织本身中生长。此外,乳腺及其周围区域的微生物群可能影响治疗效果,并作为早期检测和分期乳腺癌的潜在指标。现在已经明确,一些病原性感染,如乙肝病毒、丙肝病毒、人类乳头瘤病毒和幽门螺杆菌(Helicobacter pylori),是重要的致癌因子。肠道微生物的多样性和组成可能通过调控全身雌激素水平和炎症来影响乳腺癌的发病几率。由于能够分解雌激素和其他内源性激素的细菌变化,循环雌激素水平升高,最终增加了乳腺癌发展的风险。此外,乳腺癌患者中甲基杆菌(Methylobacterium)丰度降低与更具侵袭性的肿瘤发展有关。
革兰氏阴性细菌产生的细胞致死扩张毒素(CDT)是一种具有DNA酶活性的毒素。当这种毒素靠近胃肠道上皮时,它会导致上皮细胞的双链DNA断裂,促使细胞周期暂时停止,从而允许可能导致癌症发展的突变出现。大肠杆菌(Escherichia coli)和空肠弯曲菌(Campylobacter jejuni)均能生成CDT。致病细菌可以通过引起氧化应激间接诱导致癌作用。例如,幽门螺杆菌(H. pylori)和脆弱拟杆菌(Bacteroides fragilis)可能会激活人类酶类——精胺氧化酶,产生如过氧化氢等反应性氧物种,进而损害DNA。此外,包括双歧杆菌(Bilophila)、具核梭杆菌(Fusobacterium)、卟啉单胞菌属(Porphyromonas spp)、粪肠球菌(Enterococcus faecalis)也可能增强氧化环境导致DNA改变。
肥胖与肠道微生物
肠道微生物可影响吸收、脂肪储存、炎症反应等生理过程,从而导致肥胖。同时,一些细菌如Firmicutes、Bacteroidetes、Christensenellaceae、Lactobacillus、Bifidobacteria、Akkermansia等与肥胖有关,它们的相对丰度可通过饮食等方式调节。
结束语
本世纪初的二十年,肠道微生物的研究已取得了极大进展。从临床观察到先进检测技术,肠道微生物群和健康的因果关系愈发紧密。然而,仍有许多研究声称因果关系,而实际上只是证明了相关性。从相关性到因果关系的转变仍然是一个重要且必要的步骤,以更好地设计基于调节肠道微生物群或使用特定活性化合物的假定干预措施。由于组学分析方面的进步,科学界正逐渐走向个性化医疗,而微生物组时代显然是未来医学和营养方法范式转变的重要组成部分。
参考资料
肠道微生物群与健康:机制见解.https://gut.bmj.com/content/71/5/1020
人类多种疾病中肠道微生物组成的变化及其在疾病早期诊断中的意义. https://pmc.ncbi.nlm.nih.gov/articles/PMC10870805/
【相关资源】
幽门螺杆菌(Helicobacter pylori)菌株编号:HZB369015, ATCC 43504, JCM 7653
发酵乳杆菌(Lactobacillus fermentum)菌株编号:HZB361754, ATCC 14931
类球布劳特氏菌(Blautia coccoides)菌株编号:HZB359857, ATCC 29236, DSM 935, JCM 1395
粪布劳特氏菌(Blautia faecis) 菌株编号:HZB505146, DSM 27629,JCM 17205
泥栖布劳特氏菌(Blautia luti) 菌株编号:HZB607145, DSM 14534,JCM 17040
韦氏布劳特氏菌(Blautia wexlerae)菌株编号: HZB738209, DSM 19850, ATCC BAA-1564
肠鼠杆菌(Muribaculum intestinale) 菌株编号:HZB556411, DSM 28989, KCTC 15537
肠罗斯氏菌(Roseburia intestinalis) 菌株编号:HZB751549, DSM 14610, JCM 17583
嗜菊粉罗斯氏菌(Roseburia inulinivorans) 菌株编号:HZB719307, DSM 16841, JCM 17584
反刍颤杆菌(Oscillibacter ruminantium)菌株编号:HZB529887, JCM 18333, DSM 113516
瘤胃乳酸杆菌 (Ligilactobacillus ruminis) ,菌株编号:HZB358855, ATCC 29149, DSM 114966
活泼瘤胃球菌(Ruminococcus gnavus) 菌株编号:HZB357236, ATCC 14931
粪便普雷沃氏菌(Prevotella copri) 菌株编号:HZB751000, DSM 18205, JCM 13464, CCUG 58058T
毛螺菌科(Lachnospiraceae bacterium) 菌株编号:HZB488729, DSM 24404
具核梭杆菌(Fusobacterium nucleatum,菌株编号:DSM 19679, HZB428344
脆弱拟杆菌(Bacteroides fragilis) 菌株编号:HZB360517, ATCC 43860
普拉梭菌(Faecalibacterium prausnitzii) 菌株编号:HZB366920, ATCC 27766
腐败梭菌(Clostridium septicum) 菌株编号:HZB359653, ATCC 12464, NCTC 547
艰难梭菌(Clostridioides difficile),菌株编号:HZB354279, ATCC BAA-1870
霍氏厌氧丁酸菌(Anaerobutyricum hallii/ubacterium hallii) 菌株编号:HZB699717, DSM 3353, ATCC 27751
空肠弯曲菌(Campylobacter jejuni) 菌株编号:HZB368924, ATCC 33291
粪肠球菌(Enterococcus faecalis) 菌株编号:HZB358603, ATCC 19433, DSM 20478, JCM 8726
嗜黏蛋白阿克曼菌(Akkermansia muciniphila) 菌株编号:HZB705924, DSM 22959, ATCC BAA-835
香港克里斯滕森氏菌/Christensenella hongkongensis 菌株编号:HZB548178, DSM 18959,CCUG 54229T
敬请关注我们,共筑健康未来!
— 武汉市灰藻生物科技有限公司团队敬上
灰藻生物:我们期待着与客户共同成长,共同创造生命科学的未来!
更新日期:2024-12-11
#创作团队
编制人:小藻 | 审稿人:小灰
